М.Р.Каракозов
Вспомогательная вентиляция легких
поддержкой давлением на вдохе - выбор
оптимального уровня.
![]() Основными целями
искусственной вентиляции легких в интенсивной
терапии являются коррекция газообмена и
обеспечение отдыха дыхательным мышцам у больных
с острой дыхательной недостаточностью. В
последние годы круг показаний к полностью
контролируемым режимам ИВЛ в значительной мере
сузился, что связано с двумя наиболее вредными ее
следствиями - повышением внутриальвеолярного и
внутригрудного давления и атрофией дыхательной
мускулатуры при длительной вентиляции.
Одновременно стали появляться и
совершенствоваться различные методы
респираторной поддержки, имеющие целью улучшить
газообмен, сохранив и дополнив собственную
вентиляцию больного (1, 53). Независимо от
используемого принципа, респираторная поддержка
не должна мешать самостоятельному дыханию, а
последнее - растрачиваться на борьбу с аппаратом
ИВЛ. Успех возможен лишь при согласованном
взаимодействии пациента и респиратора.
Основными целями
искусственной вентиляции легких в интенсивной
терапии являются коррекция газообмена и
обеспечение отдыха дыхательным мышцам у больных
с острой дыхательной недостаточностью. В
последние годы круг показаний к полностью
контролируемым режимам ИВЛ в значительной мере
сузился, что связано с двумя наиболее вредными ее
следствиями - повышением внутриальвеолярного и
внутригрудного давления и атрофией дыхательной
мускулатуры при длительной вентиляции.
Одновременно стали появляться и
совершенствоваться различные методы
респираторной поддержки, имеющие целью улучшить
газообмен, сохранив и дополнив собственную
вентиляцию больного (1, 53). Независимо от
используемого принципа, респираторная поддержка
не должна мешать самостоятельному дыханию, а
последнее - растрачиваться на борьбу с аппаратом
ИВЛ. Успех возможен лишь при согласованном
взаимодействии пациента и респиратора.
![]() Несовершенство
представлений о патофизиологических процессах,
с одной стороны, и бурный рост медицинских
технологий, с другой, привели к разработке
большого количества вспомогательных режимов
ИВЛ. Между многими из них и нашими знаниями об их
влиянии на систему дыхания и организм больного в
целом уже сегодня существует глубокая пропасть
(45). По существу, не доказаны преимущества
какого-либо одного метода перед другими (1,16,25). С
другой стороны это означает, что успешное
применение какого-то режима вспомогательной
вентиляции в одном случае не приведет к
позитивному результату в другом, пусть даже
внешне похожем. Тогда врачу бывает полезно
владеть альтернативным методом ИВЛ.
Несовершенство
представлений о патофизиологических процессах,
с одной стороны, и бурный рост медицинских
технологий, с другой, привели к разработке
большого количества вспомогательных режимов
ИВЛ. Между многими из них и нашими знаниями об их
влиянии на систему дыхания и организм больного в
целом уже сегодня существует глубокая пропасть
(45). По существу, не доказаны преимущества
какого-либо одного метода перед другими (1,16,25). С
другой стороны это означает, что успешное
применение какого-то режима вспомогательной
вентиляции в одном случае не приведет к
позитивному результату в другом, пусть даже
внешне похожем. Тогда врачу бывает полезно
владеть альтернативным методом ИВЛ.
![]() Вспомогательная
вентиляция легких поддержкой давлением на вдохе
(Pressure Support Ventilation, PSV; Inspiratory Pressure Support, IPS) - ВПД -
появилась в середине 80-х годов и стала одним из
наиболее важных режимов вспомогательного
дыхания, широко распространившись в практике
интенсивной респираторной терапии (25,53). Ее
использование стало возможным после внедрения в
аппараты ИВЛ микропроцессоров и чувствительных
триггерных систем. В этом режиме может работать
большинство респираторов известных фирм (Drager,
Puritan-Bennett, Siemens, Engstrom, Bird, Bear, Hamilton и др.).
Вспомогательная
вентиляция легких поддержкой давлением на вдохе
(Pressure Support Ventilation, PSV; Inspiratory Pressure Support, IPS) - ВПД -
появилась в середине 80-х годов и стала одним из
наиболее важных режимов вспомогательного
дыхания, широко распространившись в практике
интенсивной респираторной терапии (25,53). Ее
использование стало возможным после внедрения в
аппараты ИВЛ микропроцессоров и чувствительных
триггерных систем. В этом режиме может работать
большинство респираторов известных фирм (Drager,
Puritan-Bennett, Siemens, Engstrom, Bird, Bear, Hamilton и др.).
![]() Идея метода
основана на следующем наблюдении: начатое при
спонтанном вдохе сокращение инспираторных мышц
продолжается независимо от искусственного
(вспомогательного) вдоха (39,62). Была высказана
гипотеза, что поддержка дыхания, основанная на
установлении в качестве независимого параметра
вентиляции давления в дыхательных путях (Paw),
должна лучше сочетаться с инспираторным усилием
больного, нежели поддержка объёмными методами
(40,48,56).
Идея метода
основана на следующем наблюдении: начатое при
спонтанном вдохе сокращение инспираторных мышц
продолжается независимо от искусственного
(вспомогательного) вдоха (39,62). Была высказана
гипотеза, что поддержка дыхания, основанная на
установлении в качестве независимого параметра
вентиляции давления в дыхательных путях (Paw),
должна лучше сочетаться с инспираторным усилием
больного, нежели поддержка объёмными методами
(40,48,56).
![]() Суть метода в том,
что аппарат реагирует на начало каждого вдоха и
доводит Paw до установленного врачом уровня, который
поддерживается в течение всей инспираторной
фазы. Переключение на выдох возникает, как
только респиратор уловит окончание
инспираторной активности. Выдох происходит
пассивно, можно применять ПДКВ. Графики
зависимости давления, потока и объёма от времени
представлены на рис.1.
Суть метода в том,
что аппарат реагирует на начало каждого вдоха и
доводит Paw до установленного врачом уровня, который
поддерживается в течение всей инспираторной
фазы. Переключение на выдох возникает, как
только респиратор уловит окончание
инспираторной активности. Выдох происходит
пассивно, можно применять ПДКВ. Графики
зависимости давления, потока и объёма от времени
представлены на рис.1.
![]() Потенциальным
преимуществом ВПД является постоянно меняющийся
в ходе вдоха поток, точнее синхронизированный с
нейрореспираторным драйвом (НРД) пациента, чем
при других методах вспомогательной вентиляции,
когда скорость потока, а также количество и объём
аппаратных вдохов фиксированы (Вспомогательная
контролируемая вентиляция, ACV; перемежающаяся
принудительная вентиляция, IMV; вентиляция со
стабильным минутным объёмом, MMV и др.)
Потенциальным
преимуществом ВПД является постоянно меняющийся
в ходе вдоха поток, точнее синхронизированный с
нейрореспираторным драйвом (НРД) пациента, чем
при других методах вспомогательной вентиляции,
когда скорость потока, а также количество и объём
аппаратных вдохов фиксированы (Вспомогательная
контролируемая вентиляция, ACV; перемежающаяся
принудительная вентиляция, IMV; вентиляция со
стабильным минутным объёмом, MMV и др.)
Функциональная характеристика ВПД.
- улавливание инспираторного усилия пациента
- достижение и поддержание заданного Paw
- улавливание окончания инспираторной активности, переключение на выдох.
ВПД можно разделить на три фазы (17) для того, чтобы легче представить, как работает респиратор в этом режиме:
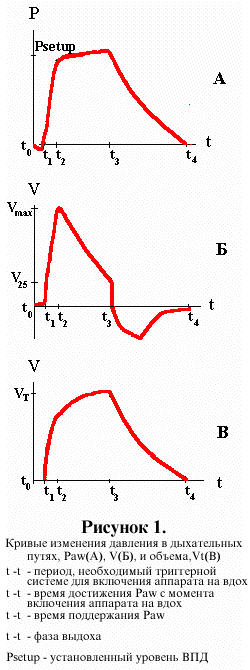
Рассмотрим их подробнее:
Улавливание инспираторного усилия. ![]() Режим
синхронизирован с каждым вдохом больного. Начало
вдоха обычно улавливается сенсором давления,
который реагирует на создавшееся в контуре
аппарата разрежение. Чем оно меньше, тем
чувствительнее сенсор. Задержка реакции
аппарата (интервал t0-t1 на рис.1)
составляет 50-250 мсек, в зависимости от
чувствительности и инерционности триггера.
Режим
синхронизирован с каждым вдохом больного. Начало
вдоха обычно улавливается сенсором давления,
который реагирует на создавшееся в контуре
аппарата разрежение. Чем оно меньше, тем
чувствительнее сенсор. Задержка реакции
аппарата (интервал t0-t1 на рис.1)
составляет 50-250 мсек, в зависимости от
чувствительности и инерционности триггера.
![]() В дополнение к
описанному триггеру по давлению, в последних
моделях некоторых аппаратов ИВЛ используется
более чувствительный потоковый триггер
"flow-by", включающий аппарат на вдох в среднем
на 25% быстрее. Описание принципа его работы
выходит за рамки обзора. Следует отметить, что
его применение при ВПД предпочтительнее (36,57)
В дополнение к
описанному триггеру по давлению, в последних
моделях некоторых аппаратов ИВЛ используется
более чувствительный потоковый триггер
"flow-by", включающий аппарат на вдох в среднем
на 25% быстрее. Описание принципа его работы
выходит за рамки обзора. Следует отметить, что
его применение при ВПД предпочтительнее (36,57)
Достижение и поддержание заданного Paw. ![]() Paw при ВПД является
главным, а в большинстве аппаратов единственным
задаваемым параметром вентиляции (не считая
чувствительности триггера, концентрации 02
в подаваемой смеси (FiO2) и ПДКВ). Как только
респиратор среагирует на вдох, высокая начальная
скорость инспираторного потока обеспечит
быстрое достижение необходимого Paw (t1-t2
на рис.1). Это давление будет поддержано (t2-t3)
в течение всей фазы вдоха (t0-t3) (10,40).
Уровень Paw можно устанавливать в пределах от 0 до
30-60 см Н2O и даже больше в некоторых
аппаратах. Скорость его достижения в большинстве
респираторов фиксирована. В аппаратах Siemens Servo 900C
и Drager Evita ее можно регулировать. Медленная
скорость достижения Paw будет отставать от усилия
больного, а слишком большая - опережать его. И то и
другое увеличит работу дыхания, но по разным
механизмам (22,24,39).
Paw при ВПД является
главным, а в большинстве аппаратов единственным
задаваемым параметром вентиляции (не считая
чувствительности триггера, концентрации 02
в подаваемой смеси (FiO2) и ПДКВ). Как только
респиратор среагирует на вдох, высокая начальная
скорость инспираторного потока обеспечит
быстрое достижение необходимого Paw (t1-t2
на рис.1). Это давление будет поддержано (t2-t3)
в течение всей фазы вдоха (t0-t3) (10,40).
Уровень Paw можно устанавливать в пределах от 0 до
30-60 см Н2O и даже больше в некоторых
аппаратах. Скорость его достижения в большинстве
респираторов фиксирована. В аппаратах Siemens Servo 900C
и Drager Evita ее можно регулировать. Медленная
скорость достижения Paw будет отставать от усилия
больного, а слишком большая - опережать его. И то и
другое увеличит работу дыхания, но по разным
механизмам (22,24,39).
Улавливание окончания инспираторной
активности и переключение на выдох. Когда
скорость потока уменьшится до 12-25% от своего
максимального значения, поддержка закончится, и
аппарат переключится на выдох (t3-t4).
Считается, что при таком соотношении
инспираторная активность прекращается (39). Кроме
того, в каждом аппарате необходимы меры
безопасности, гарантирующие переключение на
выдох, если заданное давление превышено, или
вдох слишком затянут. Последнее может
произойти, когда нарушена герметичность контура.
Из-за возникшей утечки газа респиратор не сможет
обеспечить нужное давление, вдох затянется, и
произойдет перерастяжение легких (6,16). В связи с
этим в аппарате должен быть предусмотрен предел
продолжительности вдоха, обычно равный 5
секундам.
Таким образом, ВПД является ауторегулируемым,
потокоциклическим методом вспомогательной
вентиляции легких по давлению.
![]() По мере накопления
данных о влиянии ВПД на систему дыхания,
рекомендаций к ее применению становится больше.
В настоящее время метод используется не только
для отучения от респиратора, но и в качестве
самостоятельного режима ИВЛ у больных с острой
дыхательной недостаточностью (ОДН)
По мере накопления
данных о влиянии ВПД на систему дыхания,
рекомендаций к ее применению становится больше.
В настоящее время метод используется не только
для отучения от респиратора, но и в качестве
самостоятельного режима ИВЛ у больных с острой
дыхательной недостаточностью (ОДН)
ВПД и система дыхания. ![]() Для обеспечения нормальной
альвеолярной вентиляции дыхательным мышцам
необходимо выполнить работу по преодолению
аэродинамического и эластического
сопротивления легких и грудной клетки. Во время
спокойного дыхания эта работа невелика. При
патологическом процессе сопротивление
дыхательных путей (Raw) увеличивается, а
растяжимость легких (CL) и/или грудной
клетки(СTh) уменьшается. Пытаясь сохранить
адекватную вентиляцию при возрастающей
нагрузке, дыхательные мышцы перестраиваются на
новый режим работы. Меняются градиенты
транспульмонального давления (Ptpl ), частота и
глубина дыханий (fR, VT), структура фаз
дыхательного цикла (Tins, Texp, Ttot). Несмотря на то, что
дыхательный центр стремится создать
энергетически выгодный паттерн, работа дыхания
увеличивается, кислородная цена ее растет.
Спустя определенное время, зависящее от стадии и
тяжести процесса и, в какой-то мере, от
тренированности дыхательных мышц, проявится их
усталость, и произойдет декомпенсация
вентиляции.
Для обеспечения нормальной
альвеолярной вентиляции дыхательным мышцам
необходимо выполнить работу по преодолению
аэродинамического и эластического
сопротивления легких и грудной клетки. Во время
спокойного дыхания эта работа невелика. При
патологическом процессе сопротивление
дыхательных путей (Raw) увеличивается, а
растяжимость легких (CL) и/или грудной
клетки(СTh) уменьшается. Пытаясь сохранить
адекватную вентиляцию при возрастающей
нагрузке, дыхательные мышцы перестраиваются на
новый режим работы. Меняются градиенты
транспульмонального давления (Ptpl ), частота и
глубина дыханий (fR, VT), структура фаз
дыхательного цикла (Tins, Texp, Ttot). Несмотря на то, что
дыхательный центр стремится создать
энергетически выгодный паттерн, работа дыхания
увеличивается, кислородная цена ее растет.
Спустя определенное время, зависящее от стадии и
тяжести процесса и, в какой-то мере, от
тренированности дыхательных мышц, проявится их
усталость, и произойдет декомпенсация
вентиляции.
![]() Нейромышечные
заболевания нарушают работу дыхания по другому
механизму. В этом случае мышцы по причине своей
несостоятельности с самого начала не могут
генерировать необходимый для газообмена
градиент Ptpl при здоровых легких.
Нейромышечные
заболевания нарушают работу дыхания по другому
механизму. В этом случае мышцы по причине своей
несостоятельности с самого начала не могут
генерировать необходимый для газообмена
градиент Ptpl при здоровых легких.
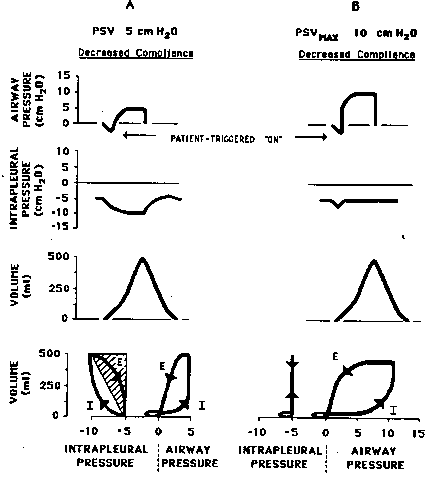
![]() Вентиляция
поддержкой давлением "разгружает"
дыхательные мышцы, модифицируя Ptpl (10,17,30,45) (рис.2).
В зависимости от выбранного уровня Paw
"разгрузка" может регулироваться от нулевой
до практически полной. Этот эффект сравним с
"разгрузкой" миокарда вазодилататорами,
дозированно снижающими общее периферическое
сопротивление и постнагрузку (18). В обоих случаях
улучшаются индексы работы, уменьшается ишемия и
усталость мышц.
Вентиляция
поддержкой давлением "разгружает"
дыхательные мышцы, модифицируя Ptpl (10,17,30,45) (рис.2).
В зависимости от выбранного уровня Paw
"разгрузка" может регулироваться от нулевой
до практически полной. Этот эффект сравним с
"разгрузкой" миокарда вазодилататорами,
дозированно снижающими общее периферическое
сопротивление и постнагрузку (18). В обоих случаях
улучшаются индексы работы, уменьшается ишемия и
усталость мышц.
![]()
![]() Являясь интерактивным
режимом дыхания, ВПД изменяет паттерн
вентиляции, что само по себе является интересным
явлением. Больной взаимодействует с
поддерживающим давлением, контролируя
скорость потока, дыхательный объём, частоту
дыхания, продолжительность фаз дыхательного
цикла (10,40). Характерно, что минутная вентиляция
(МВ) остается под контролем пациента и не
меняется в большом диапазоне давлений, о чем
свидетельствует относительное постоянство рСО2
и рН (56). Это, однако, не означает, что давление при
ВПД можно увеличивать бесконечно. Выше
определенного уровня начнется пассивное
перерастяжение легких и срыв рефлекторных
механизмов (17,34).
Являясь интерактивным
режимом дыхания, ВПД изменяет паттерн
вентиляции, что само по себе является интересным
явлением. Больной взаимодействует с
поддерживающим давлением, контролируя
скорость потока, дыхательный объём, частоту
дыхания, продолжительность фаз дыхательного
цикла (10,40). Характерно, что минутная вентиляция
(МВ) остается под контролем пациента и не
меняется в большом диапазоне давлений, о чем
свидетельствует относительное постоянство рСО2
и рН (56). Это, однако, не означает, что давление при
ВПД можно увеличивать бесконечно. Выше
определенного уровня начнется пассивное
перерастяжение легких и срыв рефлекторных
механизмов (17,34).
![]() Исследований,
посвященных влиянию ВПД на газообмен,
вентиляционно-перфузионные соотношения (V/Q),
внутрилегочный шунт не так много. При сравнении
ВПД, SIMV и вентиляции со сбросом давления в
дыхательных путях (APRV) существенных различий в V/Q
не выявлено (58). В тонком исследовании,
проведенном у хирургических больных с острым
повреждением легких, обнаружено, что ВПД
улучшает оксигенацию, если содержание
внесосудистой воды в легких не превышает 11 мл/кг
(умеренно выраженная ДН, Pa02/Fi02=125-350
mmHg). Если содержание воды больше, ВПД существенно
ухудшает V/Q и вызывает рост внутрилегочного
шунта (65).
Исследований,
посвященных влиянию ВПД на газообмен,
вентиляционно-перфузионные соотношения (V/Q),
внутрилегочный шунт не так много. При сравнении
ВПД, SIMV и вентиляции со сбросом давления в
дыхательных путях (APRV) существенных различий в V/Q
не выявлено (58). В тонком исследовании,
проведенном у хирургических больных с острым
повреждением легких, обнаружено, что ВПД
улучшает оксигенацию, если содержание
внесосудистой воды в легких не превышает 11 мл/кг
(умеренно выраженная ДН, Pa02/Fi02=125-350
mmHg). Если содержание воды больше, ВПД существенно
ухудшает V/Q и вызывает рост внутрилегочного
шунта (65).
![]() Больные с ХОЗЛ в
наибольшей степени отличаются разнообразием
регионарных механических свойств легких. Даже
тщательно подобранный уровень давления далеко
не всегда способен устранить неравномерность
вентиляции у этих больных (34,43), хотя многие
авторы свидетельствуют о хорошей переносимости
ВПД у взрослых и детей с декомпенсацией ХОЗЛ
(9,19,33,56,63). У этих больных вполне очевидна разумная
комбинация ВПД и ПДКВ для оптимизации не только
вдоха, но и выдоха.
Больные с ХОЗЛ в
наибольшей степени отличаются разнообразием
регионарных механических свойств легких. Даже
тщательно подобранный уровень давления далеко
не всегда способен устранить неравномерность
вентиляции у этих больных (34,43), хотя многие
авторы свидетельствуют о хорошей переносимости
ВПД у взрослых и детей с декомпенсацией ХОЗЛ
(9,19,33,56,63). У этих больных вполне очевидна разумная
комбинация ВПД и ПДКВ для оптимизации не только
вдоха, но и выдоха.
Выбор оптимального уровня ВПД.
- Подобно другим методам респираторной поддержки дополняет недостающий объём вентиляции, причем делает это во время каждого спонтанного вдоха.
- При отучении от респиратора, а также в качестве основного режима вентиляции у больных с дыхательной недостаточностью, позволяет дозированно изменять нагрузку на дыхательные мышцы.
Вентиляция поддержкой давлением преследует
следующие цели:
![]() Следовательно,
главным критерием для грамотного проведения ВПД
должна быть активность дыхательной мускулатуры
(20,31,32,45,60).
Следовательно,
главным критерием для грамотного проведения ВПД
должна быть активность дыхательной мускулатуры
(20,31,32,45,60).
![]() Если допустить, что
режим полностью синхронизирован с усилием
больного (22) (инспираторный поток в любой момент
времени отвечает запросам организма), то, меняя
уровень Paw, можно регулировать работу дыхания (12).
Если допустить, что
режим полностью синхронизирован с усилием
больного (22) (инспираторный поток в любой момент
времени отвечает запросам организма), то, меняя
уровень Paw, можно регулировать работу дыхания (12).
![]() Авторы,
исследующие влияние ВПД на тонус дыхательных
мышц, скорее анализируют тот или иной метод
оценки их активности во время этого режима. В
литературе нет единого мнения о том, какой должна
быть оптимальная поддержка (34,35,39,40,45,53), хотя само
понятие возникло одновременно с внедрением ВПД в
практику. Это связано со следующими причинами:
Авторы,
исследующие влияние ВПД на тонус дыхательных
мышц, скорее анализируют тот или иной метод
оценки их активности во время этого режима. В
литературе нет единого мнения о том, какой должна
быть оптимальная поддержка (34,35,39,40,45,53), хотя само
понятие возникло одновременно с внедрением ВПД в
практику. Это связано со следующими причинами:
- Неизвестен оптимальный тонус дыхательных мышц во время вспомогательной ИВЛ (34,53).
- Измерение его в условиях интенсивной терапии сложно и трудоемко.
![]() Скорее
всего, врач должен подбирать необходимый уровень
давления в зависимости от поставленной цели,
будет ли это обеспечение полной или частичной
"разгрузки". Теоретически, логична точка
зрения, согласно которой оптимальный уровень
ВПД тот, при котором сохраняющаяся активность
мышц предотвратит их атрофию и в то же время не
приведет к усталости, ибо и то и другое затянет
процесс отучения от респиратора (4,5,10,20,34,35).
По-видимому, такой подход имеет смысл и для
других методов вспомогательной ИВЛ.
Скорее
всего, врач должен подбирать необходимый уровень
давления в зависимости от поставленной цели,
будет ли это обеспечение полной или частичной
"разгрузки". Теоретически, логична точка
зрения, согласно которой оптимальный уровень
ВПД тот, при котором сохраняющаяся активность
мышц предотвратит их атрофию и в то же время не
приведет к усталости, ибо и то и другое затянет
процесс отучения от респиратора (4,5,10,20,34,35).
По-видимому, такой подход имеет смысл и для
других методов вспомогательной ИВЛ.
![]() Активность
дыхательных мышц во время ВПД оценивают разными
методами, которые можно объединить в 3 группы.
Активность
дыхательных мышц во время ВПД оценивают разными
методами, которые можно объединить в 3 группы.
![]() Первая группа
включает в себя регистрацию параметров механики
дыхания (9,10,12,29,32,35,35,37,38,41,48,49,64). Измеряются
создаваемые мышцами давления - Paw,
внутриплевральное (Ppl или Pes), Ptpl, внутрибрюшное
(Pabd или Pga), трансдиафрагмальное (Pdi)), их объёмные,
временные и скоростные характеристики. С их
помощью вычисляют работу дыхания (определенные
интегралы функций давления от объёма и давления
от времени (pressure-time product, PTP)), индекс усталости
дыхательных мышц (Pmus/Pmusmaxx Ti/Ttot), коэффициент
инспираторного усилия (IEQ), сократительную
способность дыхательных мышц (dP/dt) и др. Эти
методы инвазивны, некоторые требуют
сотрудничества больного (32).
Первая группа
включает в себя регистрацию параметров механики
дыхания (9,10,12,29,32,35,35,37,38,41,48,49,64). Измеряются
создаваемые мышцами давления - Paw,
внутриплевральное (Ppl или Pes), Ptpl, внутрибрюшное
(Pabd или Pga), трансдиафрагмальное (Pdi)), их объёмные,
временные и скоростные характеристики. С их
помощью вычисляют работу дыхания (определенные
интегралы функций давления от объёма и давления
от времени (pressure-time product, PTP)), индекс усталости
дыхательных мышц (Pmus/Pmusmaxx Ti/Ttot), коэффициент
инспираторного усилия (IEQ), сократительную
способность дыхательных мышц (dP/dt) и др. Эти
методы инвазивны, некоторые требуют
сотрудничества больного (32).
![]() Вторая группа
методов заключается в спектральном анализе
электромиографического сигнала, соотношения
высокочастотной (200-400 Гц) и низкочатотной (20-90 Гц)
составляющих спектра (В/Н).
Вторая группа
методов заключается в спектральном анализе
электромиографического сигнала, соотношения
высокочастотной (200-400 Гц) и низкочатотной (20-90 Гц)
составляющих спектра (В/Н).
![]() При проведении ВПД
Brochard предлагает ориентироваться на В/Н
грудинно-ключично-сосковой мышцы (20). Уменьшение
В/Н - сдвиг в сторону низких частот - будет
свидетельствовать о растущей усталости. Есть
мнение, что электромиографический метод
информирует об этом раньше, чем изменятся
механические характеристики (32,49).
При проведении ВПД
Brochard предлагает ориентироваться на В/Н
грудинно-ключично-сосковой мышцы (20). Уменьшение
В/Н - сдвиг в сторону низких частот - будет
свидетельствовать о растущей усталости. Есть
мнение, что электромиографический метод
информирует об этом раньше, чем изменятся
механические характеристики (32,49).
![]() Третья группа
объединяет параметры, в той или иной степени
коррелирующие с работой дыхания. Сюда входит
оценка кислородной цены дыхания (КЦД), измерение
НРД, паттерна вентиляции, наблюдение за дыханием
больного.
Третья группа
объединяет параметры, в той или иной степени
коррелирующие с работой дыхания. Сюда входит
оценка кислородной цены дыхания (КЦД), измерение
НРД, паттерна вентиляции, наблюдение за дыханием
больного.
![]() КЦД - хороший
маркер активности дыхательной мускулатуры
(9,28,51,59), но ее измерение и интерпретация
представляют проблемы в связи с постоянными
изменениями метаболизма у больных в критическом
состоянии.
КЦД - хороший
маркер активности дыхательной мускулатуры
(9,28,51,59), но ее измерение и интерпретация
представляют проблемы в связи с постоянными
изменениями метаболизма у больных в критическом
состоянии.
![]() Наблюдение за
дыханием больного - метод субъективный, но при
опытном подходе весьма полезный. Рекомендуется
следить за экскурсиями грудной клетки и живота, а
также пальпировать грудинно-ключично-сосковые
мышцы (41,53)), которые, как известно, в спокойном
дыхании участия не принимают, активизируясь
только во время нагрузок.
Наблюдение за
дыханием больного - метод субъективный, но при
опытном подходе весьма полезный. Рекомендуется
следить за экскурсиями грудной клетки и живота, а
также пальпировать грудинно-ключично-сосковые
мышцы (41,53)), которые, как известно, в спокойном
дыхании участия не принимают, активизируясь
только во время нагрузок.
![]() Анализ паттерна
вентиляции для подбора необходимого уровня ВПД
исторически был предложен первым (40). В 1986 г. McIntyre
высказал точку зрения, согласно которой
оптимальным является давление, обеспечивающее
при ВПД минимальную активность дыхательных мышц.
Дыхательный объём (VT) при этом приблизительно
равен 10-12 мл/кг, а частота дыханий (fR) около 16
в минуту. В дальнейшем было показано, что даже
комплексный анализ составляющих дыхательного
паттерна(fR,VT,fR/VT,Tins/Ttot) позволяет
судить о работе дыхания во время ВПД не более чем
наполовину, свидетельствуя о том, что
дыхательные рефлексы при поддержке давлением в
той или иной степени нарушаются (11). Тем не менее, fR
остается удобным, хотя и неточным ориентиром. Как
уже отмечалось, МВ находится под контролем
больного и как критерий подбора уровня
использоваться не должна (17).
Анализ паттерна
вентиляции для подбора необходимого уровня ВПД
исторически был предложен первым (40). В 1986 г. McIntyre
высказал точку зрения, согласно которой
оптимальным является давление, обеспечивающее
при ВПД минимальную активность дыхательных мышц.
Дыхательный объём (VT) при этом приблизительно
равен 10-12 мл/кг, а частота дыханий (fR) около 16
в минуту. В дальнейшем было показано, что даже
комплексный анализ составляющих дыхательного
паттерна(fR,VT,fR/VT,Tins/Ttot) позволяет
судить о работе дыхания во время ВПД не более чем
наполовину, свидетельствуя о том, что
дыхательные рефлексы при поддержке давлением в
той или иной степени нарушаются (11). Тем не менее, fR
остается удобным, хотя и неточным ориентиром. Как
уже отмечалось, МВ находится под контролем
больного и как критерий подбора уровня
использоваться не должна (17).
![]() В последнее время
во время ВПД предложено использовать мониторинг
НРД. Измеренное в дыхательных путях
(окклюзионное) или пищеводе (квазиокклюзионное)
давление в первые 100 миллисекунд вдоха (Р100)
хорошо коррелирует с активностью дыхательных
мышц, в том числе и во время ВПД (7,15,31,32). Делаются
попытки разрабатывать компьютерные программы,
позволяющие врачу (открытая система) или самому
компьютеру (замкнутая) по механизму обратной
связи изменять уровень поддержки в зависимости
от величины НРД (15,32). Вполне понятно, что, являясь
интегральной величиной, Р100 не несет информации о
причинах своего изменения, и чисто механическое
увеличение или уменьшение давления может
отвлечь врача от устранения этих причин.
В последнее время
во время ВПД предложено использовать мониторинг
НРД. Измеренное в дыхательных путях
(окклюзионное) или пищеводе (квазиокклюзионное)
давление в первые 100 миллисекунд вдоха (Р100)
хорошо коррелирует с активностью дыхательных
мышц, в том числе и во время ВПД (7,15,31,32). Делаются
попытки разрабатывать компьютерные программы,
позволяющие врачу (открытая система) или самому
компьютеру (замкнутая) по механизму обратной
связи изменять уровень поддержки в зависимости
от величины НРД (15,32). Вполне понятно, что, являясь
интегральной величиной, Р100 не несет информации о
причинах своего изменения, и чисто механическое
увеличение или уменьшение давления может
отвлечь врача от устранения этих причин.
![]() То же самое
относится и к другим способам оценки работы
дыхания.
То же самое
относится и к другим способам оценки работы
дыхания.
![]() Как правило,
большинство исследований при ВПД посвящено
мышцам вдоха, хотя во время ОДН, а также ИВЛ,
особенно если она проводится неправильно, может
нарушаться и режим работы экспираторных мышц.
Например, если уровень ВПД слишком высок,
происходит перерастяжение легких, активизация
мышц выдоха и рассинхронизация больного и
респиратора. У больных ХОЗЛ это может произойти
уже при обычных уровнях поддержки (34).
Как правило,
большинство исследований при ВПД посвящено
мышцам вдоха, хотя во время ОДН, а также ИВЛ,
особенно если она проводится неправильно, может
нарушаться и режим работы экспираторных мышц.
Например, если уровень ВПД слишком высок,
происходит перерастяжение легких, активизация
мышц выдоха и рассинхронизация больного и
респиратора. У больных ХОЗЛ это может произойти
уже при обычных уровнях поддержки (34).
![]() В заключении стоит
отметить, что ВПД продолжает модифицироваться.
Время покажет, в какой степени появившиеся в 90-х
годах на ее основе режимы PPSV (55), VAPSV (8,14), PAV (47,61)
нужны больному, а в какой являются данью моде и
техническому прогрессу.
В заключении стоит
отметить, что ВПД продолжает модифицироваться.
Время покажет, в какой степени появившиеся в 90-х
годах на ее основе режимы PPSV (55), VAPSV (8,14), PAV (47,61)
нужны больному, а в какой являются данью моде и
техническому прогрессу.
ПРИЛОЖЕНИЕ (из 22, с дополнениями).
Некоторые практические рекомендации для
проведения ВПД.
- При проведении ВПД следует использовать наиболее чувствительные триггерные системы.
- У трахеостомированных и интубированных больных минимальный уровень давления поддержки - 5 и 10 см Н20, соответственно. Этот уровень компенсирует работу дыхания, связанную с преодолением сопротивления контура и клапанов респиратора и рекомендуется для поддержки спонтанных вдохов как во время самостоятельного дыхания, так и во время SIMV (4,30,42,44,50).
- Давления 15-20 см Н20 обычно хватает для вентиляции и полной компенсации работы дыхания у послеоперационных (в том числе кардиохирургических) больных со здоровыми легкими и восстановленным НРД.
- Давления до 30 см Н20 практически не оказывают вредного воздействия на гемодинамику, в том числе у больных после кардиохирургических операций (2,27,40,46,58).
- Давления выше 40 см Н20 при ВПД использовать не рекомендуется.
- Проводя ВПД следует удерживать дыхание больного в "зоне комфорта", с fR 12-28 в минуту и VT больше минимально допустимого.
- При отучении от респиратора уменьшать уровень ВПД на 2 см Н2О каждые 30 мин, если больной дышит в "зоне комфорта".
- Никогда не следует уменьшать уровень поддержки ночью, за исключением случаев альвеолярной гипервентиляции.
- Если больной дышит в "зоне комфорта" при минимальных уровнях поддержки, ПДКВ<5 см Н2О и стабильной гемодинамике не менее одного-двух часов, то он готов к экстубации.
- Во время проведения ВПД следует следить за герметичностью контура аппарата и его контакта с дыхательными путями (раздутая манжета, плотно прижатая маска).
- У больных с декомпенсацией ХОЗЛ и синдромом острого повреждения легких (СОПЛ) в тяжелых стадиях ВПД следует использовать с осторожностью. Разнообразные и часто меняющиеся механические свойства легких у этих больных могут потребовать своевременного изменения уровня поддержки. Рекомендуется комбинировать ВПД с ПДКВ, в первом случае для пассивизации выдоха, во втором - для увеличения функциональной остаточной емкости.
Список литературы
- Зильбер А.П. Этюды критической медицины. т.2, 1996,
Петрозаводск
- Казеннов ВВ, Ладыгин СС, Желтов ИП, Салман НВ.
Оценка системы транспорта кислорода у
кардиохирургических больных в процессе перевода
на спонтанное дыхание. Материалы докладов 5-го
Всероссийского съезда анестезиологов и
реаниматологов. Вестник интенсивной терапии, 1996,
т.2,стр.75
- Ладыгин СС, Казеннов ВВ, Желтов ИП, Морозов МЕ.
Применение вспомогательных режимов у больных с
респираторным дистресс-синдромом после
длительной ИВЛ. Там же, стр.41
- Николаенко ЭМ, Неверин ВК, Марченков ЮВ.
Вентиляционный паттерн и функции внешнего
дыхания на этапах тренировки больных к
самостоятельному дыханию в условиях ВЛПИД после
длительной ИВЛ. Там же, стр.75
- Николаенко ЭМ, Грищенко АВ, Салтан СА, Степанов
СА, Фомичева АВ.Вентиляция легких с поддержкой
инспираторного давления.Там же, стр.76
- Aboul-Shala N, Meduri U. Noninvasive mechanical ventilation in patients with acute
respiratory failure. Crit Care Med 1996, 24:705-715.
- Alberti A, Gallo F, Fongaro A, Valenti S, Rossi A. P 40,1 0 is a useful parameter in
setting the level of pressure support ventilation. Intensive Care Med. 1995, 21(7):547-553
- Amato MB, Barbas CS, Bonassa J, Saldiva PH, Zin VA, deCarvalho CR. Volume-assured
pressure support ventilation (VAPSV). A new approach for reducing muscle workload during
acute respiratory failure. Chest, 1992, 102(4):1225-1234.
- Annat.,G.J., P.Viale, C.P.Derymez, Y.M.Bouffard, B.X.Delafosse, J.P.Motin. Oxygen cost
of breathing and diaphragmatic pressure-time index. Measurement in patients with COPD
during weaning with PSV. Chest 1990, 98:411-414 Banner MJ, Kirby RR, MacIntyre NR. Patient
and ventilator work of breathing and ventilatory muscle loads at different levels of PSV.
Chest 1991, 100:531-533
- Banner MJ, Kirby RR, Kirton OC, DeHaven CB, Blanch PB. Breathing frequency and pattern
are poor predictors of work of breathing in patients receiving pressure support
ventilation. Chest 1995, 108(5): 1338-1344.
- Berger KI, Sorkin IB, Norman RG, Rapoport DM, Goldring RM. Mechanism of relief of
tachypnea during pressure support ventilation. Chest, 1996, 109(5): 1320-1327
- Beydon L, Chasse M, Harf A, Lemaire F. Inspiratory work of breathing during spontaneous
ventilation using demand valves and continuous flow systems. Am Rev Respir Dis 1988,
138:300-304
- Branson RD, McIntyre NR. Dual-control modes of mechanical ventilation. Respir Care,
1996, 41(4):294-305
- Braschi A, Iotti G., Palo A, et.al.. Servocontrol of PS: A study on open loop response.
Abstr. Am.Rev.Respir.Dis. 1992, 145:A523
- Brochard L. Pressure limited ventilation. Respir Care 1996, 41(5):447-451
- Brochard L Pressure support ventilation In "Principles and practice of mechanical
ventilation", 1994, ed.by M.J.To-bin, McGraw-Hill, pp. 239-253
- Brochard, L, F. Pluskwa, F. Lemaire. Improved efficacy of spontaneous breathing with
inspiratory pressure support. Am. Rev. Respir. Dis., 1987, 136:411-415
- Brochard L, Rauss A, Benito S, Conti G, Mancebo, Rekik N Gasparetto A, Lemaire F.T.
Comparison of three methods of gradual withdrawal from ventilatory support during weaning
from mechanical ventilation [see comments] Am JRespir Crit Care Med 1994, 150(4):896-903
- Brochard L., A.Harf, H.Lorino, F.Lemaire, Inspiratory pressure support prevents
diaphragmatic fatigue during weaning from mechanical ventilation. Am.Rev.Respir.Dis.1989,
139:513-521
- Chui PT, Joynt GM, Oh TE. Severe hyperventilation and respiratory alkalosis during
pressure-support ventilation: report of a hazard. Anaesthesia 1995; 50(11):978-80
- Cohen IL, Bilen Z, Krishnamurthy S. The effects of ventilator working pressure during
pressure support ventilation. Chest 1993, 103(2):588-92
- Croci M, Pelosi P, Chiumello D, Gattinoni L. Regulation of pressurization rate reduces
inspiratory effort during pressure support ventilation: a bench study. Respir Care 1996,
41(10):880-4
- Dekel B, Segal E, Perel A, Pressure support ventilation. Arch Intern Med. 1996, 156(4):
369-373
- Dojat M, Harf A, Touchard D, Laforest M, Lemaire F, Brochard L.Evaluation of a
knowledge-based system providing ventilatory management and decision for extubation. Am J
Respir Crit Care Med 1996, 153(3): 997-1004
- Dries DJ, Kumar P, Mathru R, Zecca A, Rao TL, Freeark RJ. Hemodynamic effects of
pressure support ventilation in cardiac surgery patients. Am Surg 1991 Feb;57(2):122-5
- el-Khatib MF, Chatburn RL, Potts DL, Blumer JL, Smith PG Mechanical ventilators
optimized for pediatric use decrease work of breathing and oxygen consumption during
pressure-support ventilation [see comments] Comment in: CritCare Med 1995, 23(11):1931-3.
Crit Care Med 1994,22(12):1942-8
- Grassino AE. Invited editorial on "Effects of fenoterol on inspiratory effort
sensation and fatigue during inspiratory threshold loading". J Appl Phisiol 1996,
80(3): 725-726.
- Hurst JM, Branson RD, Davis K Jr, Barrette RR. Cardiopulmonary effects of pressure
support ventilation. Arch Surg 1989 Sep;124(9):1067-70
- Iotti GA, JX Brunner, A Braschi, T Laubscher, MC Olivei, A Paloet.al. Closed-loop
control of airway occlusion pressure at 0,1 sec (P 40,1 0) applied to PSV: algorithm and
application in intubated patients. Crit Care Med 1996, 24(5):771-779
- Iotti GA, Braschi A, Brunner JX, et.al. Respiratory mechanics by least square fitting in
mechanically ventilated patients: application during PSV. Intensive Care Med 1995.
21:406-413
- Jounieaux V, Duran A, Levi-Valensi P. Synchronized intermittent mandatory ventilation
with and without pressure support ventilation in weaning patients with COPD from
mechanical ventilation. Chest 1994, 105(4):1204-10
- Jubran A, WB Van de Graaff, MJ Tobin. Variability of patient-ventilator interaction with
PSV in patients with COPD. Am.J.Respir.Crit.Care Med., 1995. 152:129-136
- Kimura T, J Takezava, K Nishivaki, Y Shimada. Determination of the optimal pressure
support level evaluated by by measuring transdiaphragmatic pressure. Chest.
1991,100:112-117
- Konyukov Y, Takahashi T, Kuwayama N, Hotta T, Takezawa J, Shimada Y Estimation of
triggering work of breathing. The dependence on lung mechanics and bias flow during
pressure support ventilation. Chest 1994, 105(6):1836-41
- Kreit JW, Capper MW, Eschenbacher WL. Patient work of breathing during pressure support
and volume-cycled mechanical ventilation. Am J Respir Crit Care Med 1994,149(5):1085-91
- Lofaso F, Brochard L, Hang T, Lorino H, Harf A, Isabey D. Home versus intensive care
pressure support devices. Experimental and clinical comparison. Am J Respir Crit CareMed
1996, 153(5): 1591-1599.
- MacIntyre NR, L Ho. Effects of initial flow rate and breath termination criteria on PSV.
Chest 1991, 99:134-38
- MacItyre, NR 1989, Respiratory function during PSV. Chest 1986,89:667-683
- Monitoring in anesthesia and critical care medicine. Ed. by CD Blitt and RL Hines. 1995.
Churchill Livingstone, NY.
- Nathan SD, AM Ishaya, SK Koerner, MJ Belman. Prediction of minimal pressure support
during weaning from mechanical ventilation. Chest 1993, 103:1215-1219.
- Nava S, Bruschi C, Rubini F, Palo A, Iotti G, Braschi A. Respiratory response and
inspiratory effort during pressure support ventilation in COPD patients. Intensive Care
Med 1995, 21(11): 871-879.
- Pelosi P, Solca M, Ravagnan I, Tubiolo D, Gattinoni L Effects of heat and moisture
exchangers on minute ventilation, ventilatory drive, and work of breathing during
pressure-support ventilation in acute respiratory failure. Crit Care Med 1996,
24(7):1184-8
- Pesenti,A., N.Rossi, A.Calori, G.Foti, G.P.Rossi. Effects of short-term oxygenation
changes on acute lung injury patients undergoing PSV. Chest 1993, 103:1185-1189.
- Prakash O, Meij S. Cardiopulmonary response to inspiratory pressure support during
spontaneous ventilation vs conventional ventilation. Chest 1985, 88(3):403-408
- Ranieri VM, Giuliani R, Mascia L et al. Patient-ventilator interaction during acute
hypercapnia: pressure-support vs proportional-assist ventilation" J Appl Physiol,
1996, 81(1):426-436.
- Rasanen J, Leon MA, Cane RD. Adaptation of pressure support ventilation to increasing
ventilatory demand during experimental airway obstruction and acute lung injury. Crit Care
Med 1993, 21(4):562-6
- Sassoon CSH, Light RW, Lodia R, Sieck GC, Mahutte CK. Pressure-time product during
continuous positive airway pressure, pressure-support ventilation, and T-piece during
weaning from mechanical ventilation. Am. Rev. Respir. Dis., 1991, 143:469-476
- Shelledy DC, Rau JL, Thomas-Goodfellow L. A comparison of the effects of assist-control,
SIMV, and SIMV with pressure support on ventilation, oxygen consumption, and ventilatory
equivalent. Heart Lung 1995, 24(1):67-75.
- Shikora SA, MacDonald GF, Bistrian BR, Kenney PR, Benotti PN Could the oxygen cost of
breathing be used to optimize the application of pressure support ventilation? J Trauma
1992, 33(4):521-6; discussion 526-7
- Sinderby C, Lindstrom L, Grassino A. Automatic assessment of electromyogram quality. J
Appl Physiol 1995,79:1803-1815
- Sykes К. Respiratory Support, 1995, BMJ Publishing Group,London
- Takahashi E, Tateishi I. [Optimal pressure support ventilation as studied in a
mathematical model]. Kokyu To Junkan 1991, 39(6):573-7
- Takahashi T, Takezawa J, Kimura T, Nishiwaki K, Shimada Y Comparison of inspiratory work
of breathing in T-piece breathing, PSV, and pleural pressure support ventilation(PPSV).
Chest 1991, 100(4):1030-4
- Tokioka H, Saito S, Kinjo M, Kosaka F. The effect of pressure support ventilation on
auto-PEEP in a patient with asthma. Chest 1992, 101(1):285-622
- Van de Graaff, W.B., K.Gordey, S.E. Dornseif, D.J. Dries, B.S.Kleinman, P.Kumar,
M.Mathru. 1991. Presure support.
Changes in ventilatory pattern and components of the work of breathing. Chest 100:1082-1089
- Uchiyama A, Imanaka H, Taenaka N, Nakano S, Fujino Y, Yoshiya I. A comparative
evaluation of pressure-triggering and flow-triggering in pressure support ventilation
(PSV) for neonates using an animal model. Anaesth Intensive Care 1995, 23(3):302-6
- Valentine DD, Hammond MD, Downs JB, Sears NJ, Sims WR. Distribution of ventilation and
perfusion with different modes of mechanical ventilation. Am Rev Respir Dis, 1991,
143(6):1262-6
- Viale JP, Annat GJ, Bouffard YM, Delafosse BX, Bertrand OM, Motin JP. Oxygen cost of
breathing in postoperative patients. Pressure support ventilation vs continuous positive
airway pressure. Chest 1988, 93(3):506-9
- Younes M. Proportional-assist ventilation, a new approach to ventilatory support. Am Rev
Resp Dis 1992, 145:114-120
- Ward ME, Corbeil C, Gibbons W, Newman S, Macklem. Optimisation of respiratory muscle
relaxation during mechanical ventilation. Anesthesiology 1988, 69:29-35.
- Wetzel RC. Pressure-support ventilation in children with severe asthma. Crit Care Med
1996, 24(9):1603-5
- Yamada Y, Shigeta M, Suwa K, Hanaoka K. Respiratory muscle pressure analysis in
pressure-support ventilation. J Appl Physiol 1994, 77(5):2237-43.
- Zeravik J, Borg U, Pfeiffer UJ. Efficacy of pressure support ventilation dependent on
extravascular lung water. Chest 1990, 97(6):1412-9

