Gastric Emptying of Water in Obese Pregnant Women at Term
Cynthia A. Wong, Robert J. McCarthy, Paul C. Fitzgerald, Kiril Raikoff, Michael J. Avram
Anesth Analg 2007; 105: 751–5
Эвакуация воды из желудка у беременных женщин с ожирением в доношенный срок
Основание для исследования:
Здоровые небеременные и беременные пациентки могут пить чистую воду за 2 часа до индукции анестезии без какого-либо неблагоприятного эффекта на объем желудка. В этом исследовании мы провели сравнение эвакуации содержимого из желудка у беременных женщин с ожирением в доношенный срок гестации (индекс массы тела до беременности > 35 кг/м2) после приема 50 и 300 мл воды.
Методы:
у 10 беременных женщин-волонтеров с ожирением была оценена эвакуация из желудка с помощью серии ультразвуковых исследований желудка и оценки абсорбции ацетаминофена в перекрестном исследовании. После голодания в течение ночи волонтеры принимали 1,5 г ацетаминофена и 50 или 300 мл воды (выбиралось произвольно) дважды в течение 2 дней. Последовательные измерения площади поперечного сечения антрального отдела желудка были проведены с помощью ультразвукового изображения желудка, также был определен период полувыведения препарата из желудка (Т[1/2]). Были рассчитаны площадь под кривой концентрация ацетоминофена плазмы против времени (AUC), пиковые концентрации (Cmax) и время до получения пиковой концентрации (tmax) для 50 мл и 300 мл выпитой воды.
Результаты:
средний индекс массы тела (ИМТ) до беременности составил 41±9 кг/м2. Т[1/2] из желудка не различался после приема 300 мл воды при сравнении с 50 мл (23±11 минут против 32±15 минут). Здесь не было значимых различий между AUC ацетаминофена через 60, 90 или 120 минут, Cmax или tmax после приема 300 мл по сравнению с 50 мл воды.
Выводы:
эвакуация из желудка у беременных женщин с ожирением в доношенный срок не задерживается после приема 300 мл воды при сравнении с 50 мл. Антральный объем желудка после приема 300 мл воды практически равен исходному натощаковому уровню через 60 минут.
Аспирация жидкого и твердого содержимого желудка в легкие при индукции анестезии редкое, но тяжелое осложнение общей анестезии. Следовательно, пациентов традиционно просят голодать ночью для того чтобы удостовериться, что желудок пустой. Однако, часто пациентам трудно и некомфортно не есть или не пить, особенно для пациентов, запланированных на операцию на следующий день. Голодание приводит к появлению чувства жажды, голода, к несоблюдению рекомендаций, к повышенной тревожности [1], наряду с возможностью гипогликемии и обезвоживания. Результаты исследования в течение нескольких последних десятилетий у здоровых небеременных взрослых пациентов и у детей уже поддержали безопасность питья чистой воды за несколько часов перед индукцией общей анестезии [1-6]. В 2002 году мы показали, что опорожнение желудка не задерживается у здоровых беременных в доношенный срок без ожирения после приема чистых растворов (воды) при сравнении с отказом от питья (NP0) после ночного голодания [7].
Практические руководства по акушерской анестезии, одобренные делегатами американского общества анестезиологов в октябре 2006 года, предполагают, что беременные при отсутствии осложнений, подготовленные на плановое кесарево сечение, должны придерживаться предоперационного голодания как небеременные женщины [7а], например, NP0 для чистых растворов в течение 2 часов до запланированной хирургической процедуры [8]. Безопасность этой практики в акушерской популяции с ожирением достаточно не изучена; однако, акушерские руководства также устанавливают, что «пациентки с дополнительными факторами риска по развитию аспирации (например, морбидное ожирение…) могут иметь дальнейшие ограничения по пероральному приему жидкости, определенные индивидуально в каждом конкретном случае» [1].
Данные относительно опорожнения желудка в популяции с ожирением противоречивы. С помощью метода меченных изотопов различные исследования уже нашли, что эвакуация из желудка твердой пищи и растворов задерживается, не меняется или происходит более быстро у пациенток с ожирением при сравнении с «худой» популяцией [9].
Мы предположили, что опорожнение желудка у полных беременных женщин в доношенный срок после питья воды не отличается от опорожнения, наблюдаемого у таких же пациенток после ночного голодания. Целью этого исследования стало сравнение эвакуации из желудка у беременных-волонтеров с ожирением в доношенный срок после приема 50 мл воды (контроль) с опорожнением желудка после приема 300 мл воды. Мы выбрали 50 мл в качестве контрольного объема, а не соблюдение режима NP0, чтобы удостовериться, что ацетоминофен попадает в желудок.
Методы
Беременные волонтеры подписывали информированное согласие на участие в этом исследовании. Критериями исключения из исследования были: системные заболевания (кроме диабета второго типа или гестационного диабета), многоплодная беременность, индекс массы тела до беременности < 35 кг/м2, применение препаратов с известным эффектом на перистальтику или секрецию желудка и применение ацетаминофена в течение 48 часов до периода исследования. Опорожнение желудка оценивалось с помощью последовательных ультразвуковых исследований [10] и методом абсорбции ацетаминофена (парацетамола) [11]. Процедура и обоснование для применения ультрасонографии и абсорбции ацетаминофена обсуждены в деталях ранее [7].
Все пациентки были обследованы дважды с интервалом, по крайней мере, 48 часов, в период между 37 и 39 неделями беременности. Пациентки голодали в течение ночи, исследование начиналось в 07:30 утра. Проводилась катетеризация вены на руке. Катетер был подсоединен к одноразовой, герметичной, поточной системе без гепарина. Эта закрытая система позволяла восстанавливать утерянную кровь у пациентки после каждого забора. Проводился забор образца крови, выполнялось исходное ультразвуковое исследование. После чего все участницы исследования принимали 1,5 г ацетоминофена (15 мл жидкой суспензии ацетаминофена) и сразу же после этого 50 или 300 мл воды, назначение которой определялось с помощью произвольной числовой таблицы. Пациентки оставались в полусидячем положении до завершения серии ультразвуковых исследований, а затем им разрешалось сидеть прямо при получении последнего образца для исследования.
Ультразвуковые исследования (Acuson, Mountain View, California; датчик 5 МГц) были выполнены одним или двумя врачами, которые не были информированы об объеме выпитой жидкости. Один и тот же врач УЗ-диагностики выполнял исследования дважды пациентке, участвовавшей в исследовании. Пациентов располагали в положение полусидя с головным концом кровати приподнятым на 45 градусов [12]. Антральный отдел желудка оценивался как исходный (t0), а затем с 10-минутными интервалами после приема ацетаминофена в течение 60 минут. Правильная визуализация желудка была подтверждена непосредственным наблюдением поступления препарата/воды в желудок.
Площади поперечного сечения (CSA) двух участков антрального отдела желудка (дистальный антральный отдел привратника = antrumpylorus, а также проксимальный антральный отдел = antrumcorpus, ближе к зоне перехода между телом и антральным отделом) были измерены в сагиттальных плоскостях [10, 13] с помощью ультразвукового исследования. Были определены максимальный переднезадний и продольный диаметры. Кроме того, были рассчитаны CSA для каждого участка антрального отдела (тела и привратника) по формуле: CSA = (AP) (L)?/4.
Величины CSA antrumpylorus и antrumcorpus в каждой временной точке были рассчитаны как средние для дальнейшего анализа. Половинная максимальная CSA (CSA ?) была определена как: CSAmaximum – [(CSAmaximum - CSAbaseline)/2].
Период полувыведения из желудка (Т[1/2]) был определен как время от точки t0 до того момента, когда значения антральной CSA не достигли половинного максимального значения [14].
Кровь забиралась для определения концентраций ацетаминофена плазмы непосредственно перед приемом, а затем каждые 10 минут после приема ацетаминофена и воды в течение 60 минут, затем каждые 30 минут до 120 минут после t0. Концентрации ацетаминофена в плазме были определены с помощью метода хроматографии высокого уровня по Ameer с соавторами [15]; за исключением тех образцов, которые были элюированы изократично на 1,2 мл/мин с помощью мобильной фазы, состоящей из метанол-pH 5,29, 0,05 М буфера фосфата в отношении 15:85 после экстракции раствор:раствор, с помощью свежеприготовленного раствора ацетилсалициловой кислоты как внутреннего стандарта. Используя 0,25 мл части плазмы, эта проба имела чувствительность 0,5 мкг/мл с коэффициентом вариации в течение дня 5% или менее. Площади под кривой концентрация ацетаминофена против времени (AUC) были определены через 60, 90 и 120 минут с помощью правила трапеции. Кроме того, были определены пиковая концентрация (Cmax) и время до получения пиковой концентрации (tmax).
Параметром первичного исхода была AUC120. Анализ размера образца (?=0,05, сила=80%) с помощью парного t-теста на основе двойной выборки определил, что 10 пациенток необходимы для определения снижения на 600 мкг•мин/мл в AUC120 ацетоминофена от контрольного значения 1800 мкг•мин/мл, принимая стандартное отклонение = 600 мкг•мин/мл. Контрольное значение AUC120 в нашем предшествующем исследовании было 1949±606 мкг•мин/мл [7]. Это снижение AUC ацетаминофена было использовано без достаточных оснований в качестве выбранной клинически значимой задержки опорожнения желудка [16].
Антральные объемы CSA и объемы AUC ацетаминофена были сравнены с контрольными (50 мл) и лечебными (300 мл) сессиями с помощью ANOVA для повторных измерений (сессия, время). T[1/2], Cmax ацетаминофена и tmax сравнивались с помощью парного t-теста. Критерий для отклонения нулевой гипотезы был p<0,05. Данные суммированы и представлены как среднее значение ± среднеквадратическое отклонение.
Результаты
Послеоперационная физиотерапия и местное обезболивание (эпидуральная аналгезия) уменьшают частоту развития ателектазов и дыхательной недостаточности. Крайне важная ранняя послеоперационная мобилизация.
11 женщин дали добровольное согласие на участие в исследовании. Один волонтер не смог завершить исследование, так как роды произошли до второй серии исследования; следовательно, данные об этой пациентке были исключены из анализа. Характеристики оставшихся 10 объектов исследования показаны в таблице 1.
Таблица 1. Характеристики пациенток.
| Возраст (лет) | 27±3 |
| Рост (см) |
166±6 |
| Вес до беременности (кг) | 116±30 |
| Вес при беременности в доношенный срок (кг)а | 123±26 |
| ИМТ до беременности (кг/м2) | 42±9 |
| Гестация (недель)а | 37,2±0,6 |
| Сахарный диабет II типа/гестационный (n) | 0/2 |
Данные представлены как среднее значение ± среднеквадратическое отклонение.
ИМТ = индекс массы тела.
а Первый день исследования.
Средняя антральная CSA в период 0-60 минут показана на рисунке 1. Объемы желудка в точке 60 минут не отличались от исходных объемов. Парные различия в антральной CSA (300-50 мл) как функция времени показаны на рисунке 2. Они не отличались друг от друга в любое выбранное время. T[1/2] из желудка после приема 300 мл воды (23±11 минут) не отличалось от T[1/2] после приема 50 мл (32±15 минут) (p=0,23). Среднее снижение и 95% доверительные интервалы T[1/2] опорожнения желудка после приема 300 мл при сравнении с приемом 50 мл составило 8,4 (-3,4 до 20,4) минут.
Результаты анализа данных концентрации ацетаминофена в плазме суммированы в таблице 2. Здесь не было различий между AUC ацетоминофена через 60, 90 или 120 минут, Cmax ацетаминофена или tmax ацетоминофена после приема 50 мл воды.
0 = 50 мл, ? = 300 мл. 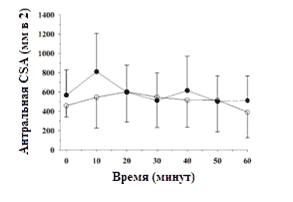 |
Рисунок 1. Средняя площадь поперечного сечения (CSA) ± среднеквадратическое отклонение (границы погрешностей) против времени для 10 обследованных пациенток.
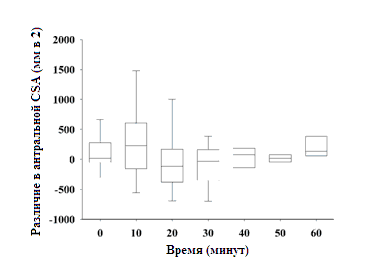 |
Рисунок 2. Срединное парное различие (300 мл – 50 мл) в антральном поперечном сечении (CSA) в зависимости от времени. Сплошная линия отражает медиану, рамка отражает IQR, а «усы» отражает 10-ю и 90-ю перцентиль. Парные различия не отличались друг от друга в любое указанное время.
Таблица 2. Показатели ацетоминофена плазмы (n=10).
| 50 мл | 300 мл | |
| AUC60 (мкг•мин/мл) | 312±248 | 296±150 |
| AUC90 (мкг•мин/мл) | 482±347 | 478±189 |
| AUC120 (мкг•мин/мл) | 622±425 | 657±204 |
| Cmax (мкг/мл) | 9,9±7,2 | 9,2±3,6 |
| tmax (мин) | 53,4±37,2 | 57,5±38,8 |
AUC = площадь под кривой через 60, 90 и 120 минут; Cmax = максимальная концентрация плазмы; tmax = время до достижения максимальной концентрации плазмы.
Обсуждение
Важность этого исследования заключается в том, что опорожнение желудка у беременных-волонтеров с ожирением в доношенный срок не различалось после приема 50 мл и 300 мл воды. Это предполагает, что руководство по голоданию для пациенток с ожирением, подготовленных на плановое кесарево сечение, не должно отличаться от руководств для пациенток с нормальным весом, и что все женщины независимо от ИМТ могут пить чистую воду за 2 часа перед плановой операцией. Это информация важна, так как распространенность ожирения устойчиво растет в беременной популяции, а женщины с ожирением имеют повышенный риск родоразрешения операцией кесарева сечения [17]. Другие факторы риска, кроме опорожнения желудка, также могут влиять на риск аспирации. Ожирение связано с более трудной масочной вентиляцией [18] и интубацией [19, 20], а также с трудным обеспечением дыхательных путей, что тоже является фактором риска для аспирации [21]. Кроме того, грыжи пищеводного отверстия и гастроэзофагеальный рефлюкс более часто встречаются у женщин с ожирением при сравнении с пациентками с нормальным весом [22]. Следовательно, ожирение может быть фактором риска для аспирации во время кесарева сечения независимо от времени опорожнения желудка.
Критическим определяющим фактором для заболеваемости и смертности, связанной с легочной аспирацией, является объем желудка и pH [23]. Несколько исследований в хирургической популяции нашли, что объемы «голодного» желудка, определенные по объему аспирата желудка, не различаются между пациентками с ожирением и с нормальным весом [24, 25]. Однако в текущем исследовании, средняя величина (± среднеквадратическое отклонение) натощаковой AUC (518±213 мм2), определенная у полных пациенток, превышала средние значения, найденные у пациенток с нормальным весом в предшествующем исследовании (407±255 мм2, средний ИМТ до беременности = 23,1±3,7 кг/м2) (p=0,02) [7]. Это и все последующие сравнения между текущем исследованием у полных женщин и нашим предшествующим исследованием у пациенток с нормальным весом должны быть интерпретированы с осторожностью, так как это два разных исследования. Другие исследователи сравнивали объем желудка у голодавших и неголодавших пациенток с ожирением, подготовленных на плановые операции [26]. Объем желудка и pH не различались у пациенток, произвольно отобранных для приема 310 мл чистой воды при сравнении с 10 мл растворов за 2 часа до плановой операции и индукции анестезии.
Данные по натощаковому pH желудка у пациенток с ожирением при сравнении с пациентками с нормальным весом - спорные. Исследования не показали различий [25], а также показали низкие значения pH у полных пациенток [24]. Несмотря на это, мы не измеряли pH в нашем исследовании, это могло не быть клинически значимым, так как акушерские пациентки рутинно получают премедикацию антацидами до индукции анестезии при хирургических процедурах [7a]. В любом случае, объем желудка и pH являются промежуточными переменными исхода, и большее исследование показано для определения - являются ли на самом деле свободные предоперационные руководства по голоданию безопасными у всех беременных женщин (с ожирением и с нормальным весом) в доношенный срок.
Значения Т[1/2] опорожнения желудка в популяции нашего текущего исследования были схожи со значениями, найденными для нормальных пациенток в нашем предшествующем исследовании с помощью такой же методологии (24±6 минут для 300 мл и 33±8 минут для 50 мл, p<0,01) [7]. Несмотря на то, что мы нашли снижение T[1/2] подобной величины после приема 300 мл при сравнении со значениями после приема 50 мл воды в текущем исследовании, различия не было статистически значимым из-за большей вариабельности. Значения Т[1/2], найденные в текущем исследовании, были схожи с измеренными у полных пациенток после приема 30-50 мл меченной радиоактивными изотопами воды (20,4 минуты) [27]. Эти исследователи также подтвердили заметную вариабельность (размах 4-80 минут) Т[1/2] опорожнения желудка.
Абсорбция ацетаминофена является непрямым методом оценки опорожнения желудка, так как ацетаминофен проходит через желудок и абсорбируется в кишечнике [28]. Надежность метода как меры оценки опорожнения желудка принимает стабильные фармакокинетические вариации [29]. Данные по абсорбции ацетаминофена в текущем исследовании у женщин с ожирением заметно отличались от данных предшествующего исследования у женщин с нормальным весом [7]. Средняя AUC120 составила примерно одну треть от нормальной популяции. AUC прямо пропорциональна дозе абсорбированного препарата, и обратно пропорциональна клиренсу выведения препарата. В текущем исследовании пациенток с ожирением Cmax было ниже, tmax было больше, чем параметры наблюдаемые в нашем более раннем исследовании у нормальных пациенток. Эти данные схожи с данными другого исследования, в котором фармакокинетика перорально назначенного ацетаминофена сравнивалась у полных пациенток с пациентками с нормальным весом [30]. В контексте настоящего исследования это предполагает, что одной из причин низкой AUC120 у наших полных волонтеров была абсорбция меньшего количества ацетаминофена через 120 минутам при сравнении с количеством, абсорбированным у пациенток с нормальным весом в нашем более раннем исследовании. Другие исследователи сравнивали фармакокинетику внутривенно назначенного ацетаминофена (для определения вариабельности, вследствие изменчивости абсорбции) у нормальных и полных больных, и нашли 50% повышение клиренса элиминации ацетаминофена у полных пациенток [31]. Это предполагает другие причины низкого AUC120 у полных волонтеров текущего исследования - повышенная элиминация при сравнении с нормальными пациентками нашего более раннего исследования.
Есть несколько недостатков плана текущего исследования и полученных результатов. Данное исследование имело недостаточную силу для определения различий AUC ацетоминофена, которое мы наблюдали. Мы брали образцы крови, так как у нас имелось более раннее исследование, и так как мы не ожидали более медленной абсорбции у этих пациенток. К сожалению, продолжительность забора образцов не была достаточной для характеристики фазы элиминации и расчета AUCinfinity у всех пациенток в текущем исследовании. AUC ацетаминофена после приема 50 или 300 мл воды у полных пациенток в нашем исследовании не различалась через 60, 90 и 120 минут, чего не было у больных с нормальным весом в более раннем исследовании [7]. Кроме того AUCinfinity ацетоминофена не различалось между сериями у пациенток с нормальным весом. Следовательно, у нас не было оснований считать, что AUCinfinity будет различаться у полных пациенток в текущем исследовании.
Учитывая повышенную вариабельность T[1/2] в текущем исследовании у полных пациенток, исследование имело недостаточную силу для определения различий в эвакуации из желудка 300 или 50 мл раствора. Дальнейшие недостатки исследования заключаются в том, что фармакокинетика ацетаминофена нарушена в популяции с ожирением, и, следовательно, его применение как непрямого метода оценки опорожнения желудка не обосновано в этой популяции пациентов.
И наконец, клинически значимый вопрос – следует ли разрешать беременным пациенткам в доношенный срок пить чистую воду за несколько часов до плановых хирургических процедур. Данные, что эвакуация из желудка 300 мл воды не удлиняется при сравнении с 50 мл, не дает прямого ответа на этот вопрос. Опорожнение желудка - это показатель риска аспирации и повышения заболеваемости. Теоретически, как нормальные, так и полные пациентки могли иметь больший объем желудка во время индукции анестезии и риск для легочной аспирации, несмотря на имеющееся время быстрого опорожнения желудка.
Таким образом, мы показали, что эвакуация жидкости желудка у беременных женщин с ожирением в доношенный срок (не в родах) не задерживается после приема 300 мл воды при сравнении с приемом 50 мл воды, и, что CSA антрального отдела желудка после приема 300 мл воды схожа с исходным натощаковым уровнем через 60 минут. Это предполагает, что разрешение полным беременным женщинам пить чистую воду за несколько часов до плановой операции может не повышать риск аспирации и последующей заболеваемости и смертности; однако, это нужно еще доказать.
Ссылки
| 1. | Agarwal A, Chari P, Singh H. Fluid deprivation before operation. The effect of a small drink. Anaesthesia 1989; 44: 632– 4. |
| 2. | Phillips S, Hutchinson S, Davidson T. Preoperative drinking does not affect gastric contents. Br J Anaesth 1993; 70: 6 –9. |
| 3. | Crawford M, Lerman J, Christensen S, Farrow-Gillespie A. Effects of duration of fasting on gastric fluid pH and volume in healthy children. Anesth Analg 1990; 71: 400 –3. |
| 4. | Goodwin AP, Rowe WL, Ogg TW, Samaan A. Oral fluids prior to day surgery. The effect of shortening the pre-operative fluid fast on postoperative morbidity. Anaesthesia 1991; 46: 1066 – 8. |
| 5. | Maltby JR, Sutherland AD, Sale JP, Shaffer EA. Preoperative oral fluids: is a five-hour fast justified prior to elective surgery? Anesth Analg 1986; 65: 1112–16. |
| 6. | Sandhar BK, Goresky GV, Maltby JR, Shaffer EA. Effect of oral liquids and ranitidine on gastric fluid volume and pH in children undergoing outpatient surgery. Anesthesiology 1989; 71: 327–30. |
| 7. | Wong CA, Loffredi M, Ganchiff JN, Zhao J, Wang Z, Avram MJ. Gastric emptying of water in term pregnancy. Anesthesiology 2002; 96: 1395– 400. |
| 7a. | American Society of Anesthesiologists Task Force on Obstetric Anesthesia. Practice guidelines for obstetric anesthesia. Anesthesiology 2007; 106: 843– 63. |
| 8. | Practice guidelines for preoperative fasting and the use of pharmacologic agents to reduce the risk of pulmonary aspiration: application to healthy patients undergoing elective procedures: a report by the American Society of Anesthesiologist Task Force on Preoperative Fasting. Anesthesiology 1999; 90: 896 –905. |
| 9. | Wisen O, Hellstrom PM. Gastrointestinal motility in obesity. J Intern Med 1995; 237: 411–18. |
| 10. | Marzio L, Giacobbe A, Conoscitore P, Facciorusso D, Frusciante V, Modoni S. Evaluation of the use of ultrasonography in the study of liquid gastric emptying. Am J Gastroenterol 1989; 84: 496 –500. |
| 11. | Clements JA, Heading RC, Nimmo WS, Prescott LF. Kinetics of acetaminophen absorption and gastric emptying in man. Clin Pharmacol Ther 1978; 24: 420 –31. |
| 12. | Carp H, Jayaram A, Stoll M. Ultrasound examination of the stomach contents of parturients. Anesth Analg 1992; 74:.683–7. |
| 13. | Bolondi L, Bortolotti M, Santi V, Calletti T, Gaiani S, Labo G. Measurement of gastric emptying time by real-time ultrasonography. Gastroenterology 1985; 89: 752–9. |
| 14. | Irvine EJ, Tougas G, Lappalainen R, Bathurst NC. Reliability and interobserver variability of ultrasonographic measurement of gastric emptying rate. Dig Dis Sci 1993; 38: 803–10. |
| 15. | Ameer B, Greenblatt DJ, Divoll M, Abernethy DR, Shargel L. High-performance liquid chromatographic determination of acetaminophen in plasma: single-dose pharmacokinetic studies. J Chromatogr 1981; 226: 224 –30. |
| 16. | Ly BT, Schneir AB, Clark RF. Effect of whole bowel irrigation on the pharmacokinetics of an acetaminophen formulation and progression of radiopaque markers through the gastrointestinal tract. Ann Emerg Med 2004; 43: 189 –95. |
| 17. | Barau G, Robillard PY, Hulsey TC, Dedecker F, Laffite A, Gerardin P, Kauffmann E. Linear association between maternal pre-pregnancy body mass index and risk of caesarean section in term deliveries. BJOG 2006; 113: 1173–7. |
| 18. | Kheterpal S, Han R, Tremper KK, Shanks A, Tait AR, O’Reilly M, Ludwig TA. Incidence and predictors of difficult and impossible mask ventilation. Anesthesiology 2006; 105: 885–91. |
| 19. | el-Ganzouri AR, McCarthy RJ, Tuman KJ, Tanck EN, Ivankovich AD. Preoperative airway assessment: predictive value of a multivariate risk index. Anesth Analg 1996; 82: 1197–204. |
| 20. | Wilson ME, Spiegelhalter D, Robertson JA, Lesser P. Predicting difficult intubation. Br J Anaesth 1988; 61: 211–16. |
| 21. | Hawkins JL, Koonin LM, Palmer SK, Gibbs CP. Anesthesia-related deaths during obstetric delivery in the United States, 1979 –1990. Anesthesiology 1997; 86: 277– 84. |
| 22. | Barak N, Ehrenpreis ED, Harrison JR, Sitrin MD. Gastro-oesophageal reflux disease in obesity: pathophysiological and therapeutic considerations. Obes Rev 2002; 3: 9 –15. |
| 23. | Mendelson C. The aspiration of stomach contents into the lungs during obstetric anesthsia. Am J Obstet Gynecol 1946; 52: 191–205. |
| 24. | Juvin P, Fevre G, Merouche M, Vallot T, Desmonts JM. Gastric residue is not more copious in obese patients. Anesth Analg 2001; 93: 1621–2. |
| 25. | Harter RL, Kelly WB, Kramer MG, Perez CE, Dzwonczyk RR. A comparison of the volume and pH of gastric contents of obese and lean surgical patients. Anesth Analg 1998; 86: 147–52. |
| 26. | Maltby JR, Pytka S, Watson NC, Cowan RA, Fick GH. Drinking 300 mL of clear fluid two hours before surgery has no effect on gastric fluid volume and pH in fasting and non-fasting obese patients. Can J Anaesth 2004; 51: 111–15. |
| 27. | Arnstein NB, Shapiro B, Ekhauser FE, Dmuchowski CF, Knol JA, Strodel WE, Nakajo M, Swanson DP. Morbid obesity treated by gastroplasty: radionuclide gastric emptying studies. Radiology 1985; 156: 501– 4. |
| 28. | Heading RC, Nimmo J, Prescott LF, Tothill P. The dependence of paracetamol absorption on the rate of gastric emptying. Br J Pharmacol 1973; 47: 415–21. |
| 29. | Gin T, Lew JK. Gastric emptying in pregnancy. Br J Anaesth 1992; 68: 115–16. |
| 30. | Lee WH, Kramer WG, Granville GE. The effect of obesity on acetaminophen pharmacokinetics in man. J Clin Pharmacol 1981; 21: 284 –7. |
| 31. | Abernethy DR, Divoll M, Greenblatt DJ, Ameer B. Obesity, sex, and acetaminophen disposition. Clin Pharmacol Ther 1982; 31: 783–90. |

