Материалы заседания круглого стола,
посвященного проблеме
послеоперационной боли и способам ее решения
Москва, 8 ноября 2005 г.
при поддержке компании Бристол Мейерс Сквибб
Современные тенденции лечения послеоперационной боли
Опубликовано в журнале доказательной медицины для практикующих врачей "Consilium medicum"
П. В. Морозов: Итак, уважаемые коллеги, насколько актуальна сегодня проблема послеоперационной боли? Какова эпидемиология острой послеоперационной боли?
А. М. Овечкин
Проблема острой послеоперационной боли существует на протяжении всего времени существования хирургии и, к сожалению, не теряет своей актуальности. Почему так происходит? Возможно, потому что в раннем послеоперационном периоде перед врачом на первом месте стоят такие задачи, как стабилизация гемодинамики, инфузионно-трансфузионная терапия, энтеральное и парентеральное питание. На этом фоне боль кажется второстепенной проблемой, неизбежной неприятностью, с которой можно смириться. Такой подход привел к тому, что сегодня лечение острой послеоперационной боли не может быть признано адекватным, причем эта проблема актуальна не только для нашей страны. На IV Конгрессе европейских ассоциаций по изучению боли было отмечено, что не менее 35% пациентов, перенесших плановые и экстренные хирургические вмешательства, страдают от послеоперационной боли. При этом в 45-50% случаев интенсивность боли является средней и высокой, а 15-20% пациентов отмечают, что интенсивность боли превысила ожидавшуюся ими.
Около 50% пациентов переводятся из интенсивной терапии в общие палаты с болями, интенсивностью свыше 5 баллов по 10-балльной шкале.

П. В. Морозов: Я хотел бы спросить: каково в целом влияние острой боли на течение послеоперационного периода?
Н. А. Осипова
Неустраненная боль у оперированного пациента сопровождается серьезными патологическими реакциями всех систем организма, которые особенно опасны при наличии сопутствующих заболеваний. Так, например, у пациентов с заболеваниями сердечно-сосудистой системы увеличивается риск инфарктов, тяжелых гипертонических кризов.
Боль нарушает многие физиологические функции (рис. 2), нарушая в том числе и заживление операционной раны. Ожидание и страх боли приводят к ограничению больным своей подвижности и как следствие - к адинамии, застойным явлениям в системе кровообращения и тромбоэмбо-лическим осложнениям. Ограничение дыхательных движений, особенно после операций на органах грудной и брюшной полости, ведет к гиповентиляции легких и развитию легочных осложнений. Таким образом, некупированная послеоперационная боль может являться причиной неудовлетворительных результатов хирургического лечения больных.
2 Комплексное влияние послеоперационной боли
ЖЕЛ - жизненная емкость легких ТЭЛА - тромбоэмболия легочной артерии А.М.Овечкин |
A. M. Овечкин
В 2000 г. были опубликованы результаты метаанализа причин летальности в хирургии по данным 35 рандомизированных контролируемых исследований (рис. 3). Было выявлено, что 45 % всех летальных исходов в послеоперационном периоде обусловлены тромбоэмболией легочной артерии (ТЭЛА), острыми инфарктами миокарда, инсультами. Указанные состояния объединяет наличие гиперкоагуляции, которая обусловлена избыточной концентрацией катехоламинов в плазме в раннем послеоперационном периоде. Гиперкатехоламинемия в свою очередь вызывается избыточной активацией симпатоадреналовой системы, вызванной болью. Именно так неадекватно купированная острая боль влияет на организм человека, на результаты хирургического лечения и выживаемость.

П. В. Морозов: Очевидно, для того чтобы понимать, как правильно лечить боль, необходимо четко представлять механизмы ее развития. Какова патофизиология острой боли?
А. М. Овечкин
Действительно, для того чтобы адекватно назначить обезболивание в послеоперационном периоде, необходимо понимать: обезболивание должно иметь патогенетический характер, т.е. быть направлено на те механизмы боли, которые лежат в основе ее формирования.
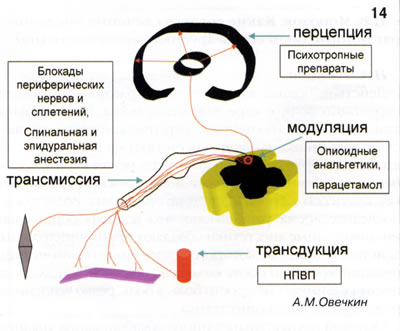
Рассмотрим современное представление о патогенезе боли. При хирургическом разрезе вокруг операционной раны формируются зоны повышенной болевой чувствительности (гипералгезии). Первичная гипералгезия развивается в зоне поврежденных тканей, где выделяющиеся из плазмы крови, поврежденных клеток и окончаний С-афферентных волокон медиаторы боли (алгогены) сенситизируют периферические ноцицепторы, снижая порог их активации.
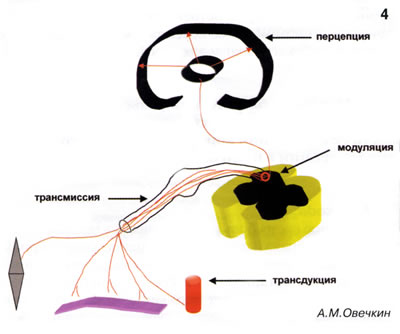
Процесс формирования болевого стимула на периферии называется трансдукцией (рис. 4). Далее запускается процесс трансмиссии: сформировавшийся болевой импульс по афферентным волокнам передается к ноцицептивным нейронам задних рогов спинного мозга. Согласно современным представлениям о патофизиологии боли, задние рога спинного мозга - ключевая структура в формировании окончательного болевого сигнала, поскольку именно там определяется его интенсивность и происходит модуляция болевого импульса. Наиболее важным механизмом контроля боли на этом уровне является эндогенная опиатная система. Нейропептиды (эндорфины и энкефалины), воздействуя на опиатные рецепторы, запускают антиноцицептивную систему, снижая интенсивность пришедшего с периферии болевого сигнала. Модулированный ноцицептивный сигнал распространяется по восходящему неоспиноталамическому пути к коре головного мозга, где происходит осознанное восприятие боли - перцепция. На уровне коры формируется также и негативный эмоциональный компонент.
На настоящий момент врачи имеют возможность воздействовать на каждый этап механизма формирования боли.
П. В. Морозов: Каковы тогда причины хронизации острой боли?
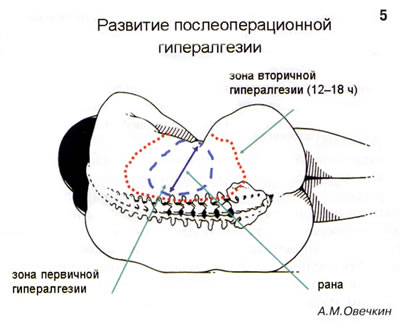
Развитие первичной гипералгезии неизбежно, и если мы в этот момент неадекватно обезболиваем пациента, то в течение 12-18 ч вне зоны повреждения формируется вторичная гипералгезия (рис. 5). Именно эти 12-18 ч раннего послеоперационного периода особенно важны для обезболивания, для положительного прогноза дальнейшего течения болевого синдрома и снижения риска его хронизации.
Вторичная гипералгезия развивается в результате включения центральных механизмов сенситизации ноцицептивных нейронов, располагающихся в задних рогах спинного мозга. Одним из основных механизмов центральной сенситизации является развитие феномена "взвинчивания" активности ноцицептивных нейронов задних рогов спинного мозга, проявляющееся прогрессивным увеличением частоты потенциалов действия, генерируемых ноцицептивными нейронами в ответ на повторную стимуляцию С-афферентов.
Чем шире образующаяся зона рецептивных полей нейронов задних рогов спинного мозга, тем интенсивнее болевой синдром и тем больше предпосылок для его хронизации.
В настоящее время выявлены причинно-следственные связи между травматичностью операции, интенсивностью послеоперационного болевого синдрома и вероятностью формирования хронического болевого синдрома. В частности, известно, что раннее развитие болевого синдрома (в течение первых 4-5 ч после операции) является прогностически неблагоприятным фактором. При некупированной острой послеоперационной боли вероятность хронизации составляет от 0,3 до 55%.
Чем выше интенсивность острой послеоперационной боли, тем выше вероятность ее хронизации, и, таким образом, наиболее перспективным потенциальным методом профилактики хронической боли является лечение острой боли.
Н. А. Осипова
Я хотела бы добавить, что в онкологии проблема хронизации боли стоит особенно остро, что связано с большим объемом оперативных вмешательств, а также наличием предоперационного болевого синдрома, обусловленного онкологическим процессом. Поэтому мы не просто лечим послеоперационную боль, а используем профилактический подход, защищая пациента от боли в предоперационном периоде до нанесения травмы (рис. 6).

А. М. Овечкин
Кроме того, хроническая послеоперационная боль имеет не только медицинское, но и социально-экономическое значение. Согласно данным, представленным американскими врачами, если у 30-летнего пациента боль стала хронической, то стоимость ее лечения к концу жизни может составить от 0,5 до 1 млн долларов США.
П. В. Морозов: Мы получили развернутое представление о патофизиологии острой боли и необходимости ее адекватной коррекции. Каковы современные тенденции в послеоперационном обезболивании?
В. В. Никода
Длительное время боль рассматривалась исключительно как проблема врача и пациента. Осознание данной проблемы в обществе привело к созданию специализированных общественных организаций. В России действует общественная организация "Совет по боли", которая объединяет ведущих экспертов в области изучения и лечения боли. Стратегическая линия деятельности совета направлена на повышение качества обезболивания в отечественном здравоохранении. Совет призван содействовать переходу российской медицины к современным технологиям и международным стандартам, внедрению высокотехнологичных методов обезболивания и инноваций в практическую деятельность российских врачей.
Однако признание проблемы боли не только обществом, но и на государственном уровне позволит приблизиться к ее решению.
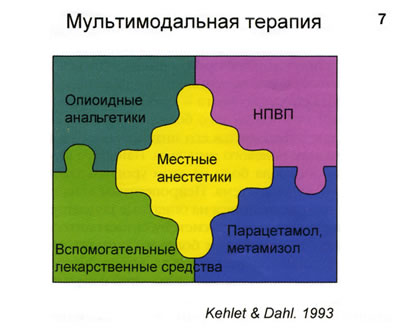
В настоящий момент существуют регионарные, европейская и международная ассоциации по изучению боли, в которых состоит огромное количество специалистов и вырабатывается консенсус по лечению боли: алгоритмы, подходы, руководства. К таким подходам относятся мультимодальная терапия (рис. 7) и поэтапное наращивание аналгезии. В последние 15-20 лет вследствие целого ряда медицинских, социальных, экономических и юридических причин наблюдается отчетливая тенденция к усилению роли неопиоидного компонента в мультимодальной аналгезии. И здесь следует отметить важную роль нестероидных противовоспалительных препаратов (НПВП), таких как парацетамол в инъекционной форме.
П. В. Морозов: Если я вас правильно понял, существуют консенсусные документы по лечению острой боли, принятые международным сообществом.
В. В. Никода
Да, существует Европейский стандарт, рекомендации Американского общества по лечению боли. Так, например, Европейский стандарт по фармакотерапии послеоперационной боли (рис. 8) предполагает ступенчатое наращивание обезболивающей терапии от стандартных общедоступных таблетированных форм неопиоидных анальгетиков до применения высокотехнологичных, современных методов обезболивания, включающих регионарное обезболивание и контролируемую пациентом аналгезию. Вместе с тем разрабатываются образовательные программы для пациентов. Следует понимать, что эффективное лечение боли возможно только при комплексном подходе: необходимо объединить усилия пациента, врача, общества и государства.

П. В. Морозов: Надежда Анатольевна, я знаю, что вы имели непосредственное отношение к созданию Российских рекомендаций. Вы не могли бы нам рассказать о них?
Н. А. Осипова
Да, в 2005 г. вышло третье издание российских методических указаний "Принципы клинического применения наркотических и ненаркотических аналгетических средств при острой и хронической боли". Целью этой работы являлось определение общих патогенетических принципов лечения и представление конкретных схем лечения наиболее распространенных вариантов острой хронической боли.
Врачи должны понимать, что задачу лечения послеоперационной боли нельзя решать по принципу "болит - значит, пора обезболивать". Следует более широко рассматривать эту проблему: как защитить пациента от боли в хирургии. И эта защита должна начинаться не в послеоперационный период, а еще до начала оперативного вмешательства, с тем, чтобы предотвратить эти процессы периферической и центральной сенситизации и гипералгезии. Только в этом случае мы сможем предотвратить тяжелую ситуацию с болевым послеоперационным синдромом и, следовательно, дальнейшую хронизацию боли. Основная тенденция клинических исследований последних лет в этой области - использование принципа мультимодяльности защиты от боли с акцентом на профилактическую защиту.
П. В. Морозов: Какие средства лечения послеоперационной боли есть в арсенале врачей сегодня?
Н. А. Осипова
Действие общих анестетиков направлено на блокаду перцепции боли в коре головного мозга. Все остальные этапы патогенеза боли при хирургической травме остаются неохваченными, общие анестетики на них не действуют. Таким образом, общий анестетик может убрать только ощущение боли, но не может модулировать патологические процессы в болевой системе организма. Более того, в последнее время установлено, что все парообразующие ингаляционные анестетики обладают проноцицептивным действием, в основе которого лежит брадикинин-индуцирующий эффект, и после выхода из общей анестезии у пациента возникает не просто боль, а боль, резко усиленная в результате действия анестетика.
Основой послеоперационного обезболивания традиционно считается системное введение опиоидных анальгетиков. Опиоидный компонент остается как основа защиты от боли на центральном (сегментарном и надсегментарном) уровне. Препараты данной группы активируют эндогенную антиноцицептивную систему (центральная аналгезия), однако не могут обеспечить полную анестезиологическую защиту. Опиоидные анальгетики не влияют на периферические и сегментарные неопиоидные механизмы ноцицепции и не предотвращают центральную сенситизацию и гипералгезию. Вот почему общие анестетики в сочетании с самыми мощными опиоидными анальгетиками полностью не способны защитить пациента от боли при операционной травме. Следовательно, следует воздействовать также на неопиоидные механизмы развития боли. Возможности такого воздействия представлены на рис. 9.
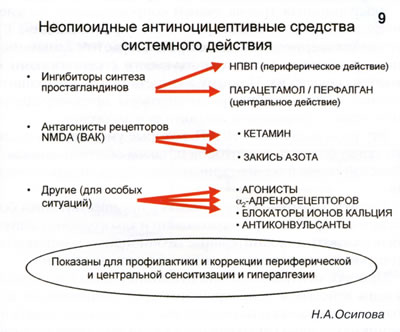
Операционная травма тканей сопровождается выделением химических медиаторов боли - простагландина Е2, сенсибилизирующего болевые рецепторы, и брадикинина, непосредственно взаимодействующего с рецепторами и возбуждающего их. Поэтому антиноцицептивную защиту организма целесообразно начинать на предоперационном этапе с применения ингибиторов алгогенов.
Эту роль выполняют НПВП, которые уменьшают сенси-тизацию болевых рецепторов и, таким образом, снижают болевой поток к сегментарным структурам спинного мозга.
Следует заметить, что у больных с предшествующим болевым синдромом, при наркомании и алкоголизме следует использовать дополнительные неопиоидные компоненты (см. рис. 9) для потенцирования эффекта аналгезии.
Процесс центральной сенситизации связан с возбуждающим действием нейротрансмиттеров (аминокислот аспартата и глутамата) на рецепторы, что приводит к закреплению состояния гипералгезии. Общий анестетик кетамин в малых дозах является антагонистом рецепторов этих нейротрансмиттеров. Наша практика показывает, что применение мультимодальной центральной аналгезии в виде комбинации опиоида и кетамина в малых дозах позволяет остановить процесс центральной сенситизации (рис. 10).

На уровне спинного мозга также существуют другие нейротрансмиттеры, в частности простагландиноподобные нейромедиаторы, которые активируются под влиянием циклооксигеназы-3 (ЦОГ-3). Препарат парацетамол способен подавлять активность ЦОГ-3, делая тем самым защиту от боли более совершенной.
Недавно был выпущен парацетамол в форме раствора для внутривенной инфузии, что позволяет применять его в терапии острой послеоперационной боли.
Первый опыт работы с Перфалганом показал его высокую эффективность, и мы будем продолжать работу с этим препаратом для определения его места в системе анестезиологической защиты пациента.
A. M. Овечкин
Важнейшее значение тканевого воспаления в механизмах центральной сенситизации, а следовательно, и в формировании хронической боли является показанием для включения в схему лечения послеоперационной боли НПВП. В течение длительного периода времени НПВП считали периферическими анальгетиками, способными через обратимую блокаду циклооксигеназы (ЦОГ) подавлять синтез медиаторов воспаления, в первую очередь простагландинов, в тканях. Затем были получены доказательства центрального действия НПВП. В частности, показано, что НПВП угнетают таламический ответ на ноцицептивную стимуляцию и препятствуют повышению концентрации простагландинов в спинно-мозговой жидкости, что тормозит развитие вторичной гипералгезии.
Здесь огромную роль сыграло исследование механизма действия парацетамола (рис. 11). При ноцицептивной стимуляции происходит сенситизация и сенсибилизация не только периферических ноцицепторов, но и ноцицепторов сегментарных на уровне задних рогов спинного мозга. Важную роль в этом процессе играют циркулирующие в спинно-мозговой жидкости простаноиды (простагландиноподобные нейромедиаторы). Оказалось, что за счет ингибирования активности ЦОГ-3 в спинно-мозговой жидкости парацетамол подавляет вторичную гипералгезию, т.е. уменьшает сенситизацию ноцицепторов задних рогов спинного мозга. Таким образом, парацетамол действует на центральные механизмы, в отличие от НПВП, основным механизмом действия которых является подавление синтеза медиаторов воспаления и боли в периферических тканях. Открытие механизма центрального действия парацетамола явилось основополагающим фактором включения данного препарата в схему послеоперационного обезболивания. Помимо высокой эффективности, важным аспектом применения парацетамола является его безопасность (рис. 12).


В. В. Никода
Надо сказать, что в Российском научном центре хирургии с этого года рутинно применяется внутривенная форма парацетамола - Перфалган. Введению Перфалгана в повседневную практику предшествовало открытое исследование послеоперационной боли. Согласно протоколу исследования пациентам в послеоперационном периоде сразу после поступления из операционной планово по 1 г 4 раза в сутки назначался Перфалган и, если требовалось, проводилось мультимодальное обезболивание другими препаратами: опиоидными и неопиоидными. Использование Перфалгана в послеоперационном периоде в качестве базисного обезболивания в комплексе мультимодальной аналгезии 89% пациентов оценили как удовлетворительное обезболивание.
A. M. Овечкин
По оценкам специалистов, адекватность опиоидной моноаналгезии даже при оптимальных режимах назначения не превышает 25-30%, так как эффективная доза близка к той, которая угнетает дыхание (рис. 13). Помимо депрессии дыхания увеличение дозы лимитировано увеличением частоты других побочных эффектов, таких как угнетение сознания, кожный зуд, затруднение самостоятельного мочеиспускания в послеоперационном периоде. С этим связана одна их основных современных тенденций в послеоперационном обезболивании - ограничение традиционного внутримышечного введения опиоидных анальгетиков.
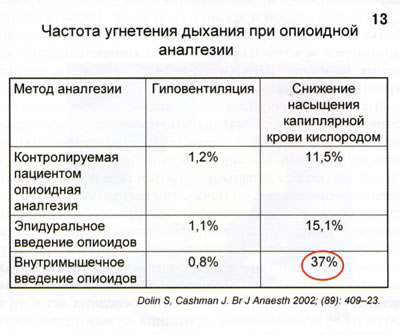
К другим современным тенденциям защиты пациента от боли относятся широкое использование неопиоидных анальгетиков (парацетамол и НПВП), применение высокотехнологичных методов послеоперационного обезболивания: продленной эпидуральной аналгезии и контролируемой пациентом аналгезии. И наконец, глобальная тенденция - это мультимодальный характер послеоперационного обезболивания.
П. В. Морозов: Вы уже неоднократно говорили о важности использования мультимодальной аналгезии. Какова ее роль и значение в послеоперационном обезболивании?
A. M. Овечкин
Мультимодальная аналгезия предусматривает одновременное использование двух или более анальгетиков, обладающих различными механизмами действия и позволяющих достичь адекватного обезболивания при минимуме побочных эффектов, присущих назначению больших доз одного анальгетика в режиме монотерапии (рис. 14).
Н. А. Осипова
Такой подход позволяет повысить безопасность обезболивания, поскольку, например, НПВП имеют широкий спектр побочных свойств, в числе которых гастротоксич-ность с возможностью развития кровотечения, нарушение функции почек и возможность увеличения операционной кровопотери. Метамизол, широко распространенный в России, может оказывать гематотоксическое действие и снижать функцию почек. Парацетамол в больших дозах обладает гепатотоксичностью. Вот почему, выбирая в каждом конкретном случае неопиоидные компоненты для повышения эффективности и увеличения безопасности опиоидной аналгезии, врач должен иметь выбор препаратов для назначения не только эффективного, но и наиболее безопасного для данного пациента лекарства.
А. М. Овечкин
На прошедшем в Вене ежегодном конгрессе "Евроанестезия -2005" были представлены данные многоцентрового исследования PATOS, в котором приняли участие 1540 клиник Европы (рис. 15). Результаты исследования показали, что при обширных абдоминальных операциях наиболее часто используются неопиоидные анальгетики: НПВП и парацетамол, которые, имея разные механизмы действия, хорошо дополняют друг друга при ранней послеоперационной аналгезии. При необходимости используется продленная эпидуральная аналгезия местными анестетиками и опиоидами.
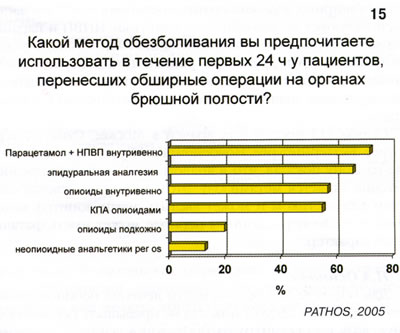
Опрос 313 российских врачей в Москве, Санкт-Петербурге, Екатеринбурге, Новосибирске, Краснодаре и Ростове-на-Дону показал, что в аналогичной ситуации предпочтение отдается метамизолу. Этот препарат является слабым анальгетиком и может вызвать агранулоцитоз, который в послеоперационном периоде может иметь фатальный характер.
Н. А. Осипова
Для обеспечения безопасности лечения неопиоидными анальгетиками следует никогда не превышать рекомендуемую дозу, всегда учитывать противопоказания и не применять их в течение длительного времени.
A. M. Овечкин
Возвращаясь к мультимодальной аналгезии, хочу сказать, что сегодня в арсенале врача есть препараты, которые воздействуют на все уровни формирования болевого синдрома (рис. 16). В нашей практике мы применяем следующую схему эффективной мультимодальной аналгезии.
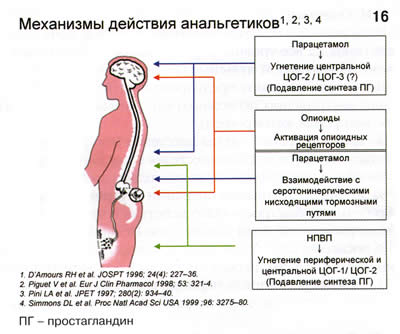
Исходя из принципа предупреждающей аналгезии, согласно этой схеме рекомендуется за 30-40 мин до операции, лучше внутривенно, но можно и внутримышечно, ввести нестероидный противовоспалительный препарат (лорноксикам, кеторолак, кетопрофен).
Во время операции схемы анестезии могут быть различными, в зависимости от степени ее травматичности. Но мы считаем, что регионарная анестезия в том или ином варианте (инфильтрация краев раны, блокада нервов и сплетений, спинальная или эпидуральная анестезия) должна присутствовать в обязательном порядке.
За 30 мин до окончания операции внутривенно вводится 1 г парацетамола в течение 15 мин. Инфузия парацетамола обеспечивает быстрое начало действия - через 5 мин после его введения определяется снижение интенсивности послеоперационной боли у пациентов. Целью применения парацетамола является снижение интенсивности боли в ранний послеоперационный период, который определяет дальнейший прогноз развития послеоперационного болевого синдрома. Пациент должен проснуться без боли. И предлагаемая методика позволяет решить эту задачу.
В послеоперационном периоде возможны различные варианты обезболивания в зависимости от травматичности операции и течения послеоперационного периода (рис. 17).
Н. А. Осипова
Следует сказать, что к моменту пробуждения пациента после наркоза, после окончания действия не только общего анестетика, но опиоидного анальгетика, развивается острая гипералгезия. И важно именно в этот момент использовать базовую неопиоидную аналгезию, включающую комбинацию НПВП и парацетамола. Это позволит избежать назначения опиоида в ранний послеоперационный период, когда важно активизировать дыхание.
Потребность в опиоиде на фоне базовой послеоперационной аналгезии НПВП или Перфалганом снижается на 30-50%.
В. В. Никода
Сегодня для всех очевидно, что нет идеального анальгетика, который бы воздействовал на все механизмы развития боли. Качество обезболивания - это соотношение хороших результатов обезболивания к частоте нежелательных явлений, которые возникают при применении тех или иных анальгетиков. Чтобы повысить качество обезболивания, необходима комбинация лекарств и методов обезболивания.
В нашей практике сразу же при поступлении пациента из операционной, ему в качестве базисного обезболивания вводятся неопиоидные анальгетики. При отсутствии противопоказаний - Перфалган (внутривенный парацетамол) в суточной дозе до 4 г. Если обезболивание недостаточно, то назначается нестероидный противовоспалительный препарат лорноксикам в суточной дозе 16-24 г в сутки. При отсутствии необходимого эффекта, мы применяем опиоидные анальгетики в виде контролируемой пациентом аналгезии или стандартно по показаниям. Наш опыт свидетельствует, что доза опиоидных анальгетиков при такой схеме ниже, чем при монотерапии опиоидными препаратами (рис. 18).
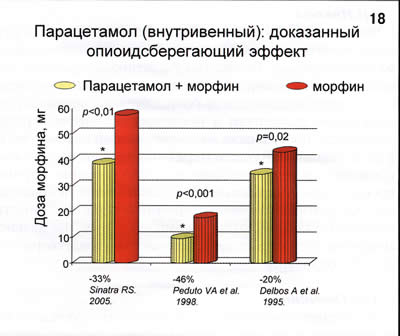
А. М. Овечкин
Внедрение принципа мультимодальной аналгезии дает ощутимый экономический эффект за счет сокращения сроков пребывания в клинике, в первую очередь в отделении реанимации и интенсивной терапии, ранней реабилитации и активизации пациента, а также снижения частоты послеоперационных осложнений.
П. В. Морозов
Подводя итоги нашей сегодняшней встречи, можно ли сказать, что вы на правильном пути и видите хорошие перспективы решения проблемы защиты пациента от боли в хирургии?
Н. А. Осипова
Мы уже сейчас решаем эту проблему. В нашей клинике пациенты после обширных операций хорошо себя чувствуют и их не беспокоит боль. Значит, уже сейчас есть результат. Важно помнить, что система защиты пациента от боли должна работать, начиная от первого прикосновения скальпеля к пациенту и на протяжении всего послеоперационного периода.
A. M. Овечкин
К сожалению, проблема решения острой послеоперационной боли далека от своего решения как в России, так и за рубежом. В сознание врачей нужно внедрить мысль, что достижение адекватного послеоперационного обезболивания возможно лишь при использовании принципов мультимодальной сбалансированной аналгезии. И здесь будет уместно привести слова немецкого профессора Джаге: «План анестезии без плана последующей аналгезии является несостоятельным...».
П. В. Морозов:
Завершая заседание круглого стола, я хочу вам напомнить одно латинское изречение, которое может служить девизом работы всех врачей: "Regens defendum" - "Управляя - защищай". Я думаю, наши коллеги, участники заседания, в полной мере продемонстрировали как можно достичь этого уже сегодня. Спасибо вам, берегите себя.

