Водно-иммерсионная компрессия
Отрывок из книги А. П. Зильбера, Е. М. Шифмана "Акушерство глазами анестезиолога"
Как было отмечено выше, метод водно-иммерсионной компрессии (ВИК) широко используется нами для лечения отёчного компонента преэклампсии и коррекции гемодинамики путём смещения внесосудистой жидкости в кровоток.
Краткая история проблемы
Прогресс в медицине, как впрочем и в других областях человеческих знаний, нередко связан с возвращением к прошлому опыту и его переосмыслением. Бальнеология (от лат. balneum – ванна), или гидротерапия является старым, хорошо известным терапевтическим методом. Почти во всех памятниках письменности древних цивилизаций можно встретить упоминания о целебных свойствах воды, применяемой разными методами и при разных режимах [19]. Погружение в воду как средство гидротерапии прошло долгий путь от гигиенического и культового применения до эффективного метода в комплексе интенсивной терапии преэклампсии.
В конце XVIII в. вышла в свет книга баварского монаха Себастьяна Кнейпа «Моё водолечение, испытанное в продолжении более 40 лет и предлагаемое мною для излечения болезней и поддержания здоровья», выдержавшая более 60 изданий. Среди многих благотворных эффектов гидротерапии при лечении различных заболеваний автор приводит свои наблюдения по использованию метода при некоторых осложнениях беременности.
В 1847 г. H.Hartshorne [134] описал диуретический эффект при погружении в воду и предложил вероятный механизм действия, в основе которого лежало перераспределение крови, возникающее после погружения в воду. Он предположил существование рецепторов в полостях сердца, реагирующих на степень наполнения и изменяющих уровень экскреции воды почками. Таким образом, он предвосхитил открытие волюмрецепции, предсердного натрийуретического полипептида и функциональной связи между почечной и внутрисердечной гемодинамикой. Тем не менее, большинство клиницистов и физиологов в течение последующих ста лет оставались равнодушными к результатам этих исследований, или, возможно, не знали о них.
В 1924 г. группа исследователей под руководством H.C.Bazet [59] изучала влияние погружения в воду на функцию почек и пришла к выводу, что погружение в воду стимулирует диурез и у здоровых людей, и при различной патологии.
В последние три десятилетия возродился интерес к роли различных рецепторов и закона Франка-Старлинга в регуляции объёма внутрисосудистой жидкости при гиповолемии. Толчком к этому послужило развитие медицины критических состояний, переосмысление роли эндотелиального повреждения при таких состояниях как сепсис, ожоговая болезнь и эклампсия. Началом стали исследования O.H.Gauer и J.P.Henry, (1963), изучавших физиологические реакции перераспределения кровотока. Сегодня, рассуждая об эффектах увеличения притока крови к органам грудной клетки, уже мало кто вспоминает, что основным инструментом авторов при моделировании увеличения венозного возврата было погружение в воду. Сами авторы отмечали, что погружение тела в воду по шею – это удобный метод для изучения жидкостного перераспределения в организме [114].
Многие исследователи изучали физиологические эффекты погружения в воду, но в большинстве своём они были не клиницистами, а специалистами, работающими в области аэрокосмической биологии и медицины. Освоение человеком космоса выявило много физиологических следствий невесомости: увеличение диуреза, натрийуреза, потерю веса и др. Эти эффекты связывают с перераспределением кровотока в условиях, когда отсутствует земное притяжение. Механизм этих явлений до конца не выяснен, но установлено, что все они сопровождаются увеличением ОЦК и преднагрузки сердца. И хотя физиологические эффекты погружения в воду нельзя полностью отождествлять с влиянием невесомости, тем не менее на протяжении нескольких десятилетий специалисты, работающие в области аэрокосмической биологии и медицины использовали этот метод для воспроизведения многих «космических» эффектов.
Ставшие классическими исследования M.Epstein [103] объясняли отдельные механизмы натрийуретического и диуретического эффектов при погружении в воду как гормональные реакции системы ренин-ангиотензин-альдостерон, АДГ и др. В 1992 г. выходит блестящий обзор того же автора, в котором подводится итог пятнадцатилетнего опыта изучения погружения в воду [104].
Тем не менее, клиницисты и до сих пор не стремятся использовать этот простой метод для лечения нарушений водного баланса, хотя за последние два десятилетия несколько групп исследователей занимались изучением и разработкой различных аспектов водно-иммерсионной компресии. Терапевтический эффект погружения в воду был подтверждён при исследовании больных циррозом печени, артериальной гипертензией, нефротическим синдромом, пересадки почек, инфарктом миокарда и др. [131, 190]. Погружение в воду с успехом используется при лечении ожоговой болезни, когда площадь ожогов составляет от 50 до 78% [189]. При физиологических исследованиях эффекта погружения в воду метод называли погружение в воду по шею (head out water immersion). Наиболее распространённое название метода при его клиническом использовании – водно-иммерсионная компрессия (ВИК).
Обращение к этому методу выглядит оправданным даже с позиций филогенеза. Когда наши одноклеточные, а затем многоклеточные предки, пройдя все тяготы эволюции, вышли из воды на сушу, им потребовалось создать сложную систему регуляции постоянства объёма и состава внутренней жидкой среды. Потребовались механизмы поддержания состава и объёма внутриклеточной и внеклеточной жидкости вне зависимости от свойств окружающей среды. Филогенетически эта система регуляции наиболее древняя, и неудивительно, что у человека она настолько совершенна, что даже при возникновении критических состояний сохраняет жизнеспособность довольно длительное время.
Следовательно, погружение в воду никак не может считаться противоестественным для регуляции функций организма, древние предки которого вышли из воды, если главное изобретение эволюции – дыхание воздухом – не нарушается. Речь идёт не о родах в воде и не об уринотерапии – мы не имеем ни опыта, ни знаний по этим экзотическим (напомним, что греч. слово экзотика – exwtismoV/экзотикос – означает чуждый, иноземный) увлечениям парамедицины. Мы рассуждаем лишь об использовании метода погружения в воду для воздействия на жидкостную регуляцию организма, и в частности – для стимуляции диуреза и борьбы с отёчным синдромом.
Метод ВИК – водно-иммерсионной компрессии – состоит в погружении больных в ванну, заполненную водопроводной водой термонейтральной температуры (34o) до уровня VI шейного позвонка. Сеанс пребывания в воде продолжается 1,5-2 часа. Как было установлено нашими исследованиями, оптимальное количество сеансов – 6-8 (до 10), ежедневно или через день. ВИК применялась в комплексе лечения 724 беременных с преэклампсией. Диагноз преэклампсии и степень тяжести определяли согласно разработанным алгоритмам диагностики, рассмотренным в предыдущей главе. У всех больных из комплекса лечения были исключены инфузионная терапия и применение диуретиков, следовательно, результаты воздействия на жидкостный баланс должны быть отнесены только к эффектам ВИК.
Исследовались показатели центральной гемодинамики, гемоглобина (Гб), гематокрита (Гт), ОЦК и ОЦП, концентрация общего белка в плазме, электролиты в плазме и моче (Na+, K+, Ca++). Исследования проводили при поступлении в родильный дом (I), после пятого (II) и десятого (III) сеансов ВИК.
Изменения кровообращения
Предполагаемый механизм действия водно-иммерсионной компресии представлен на рис. 25.
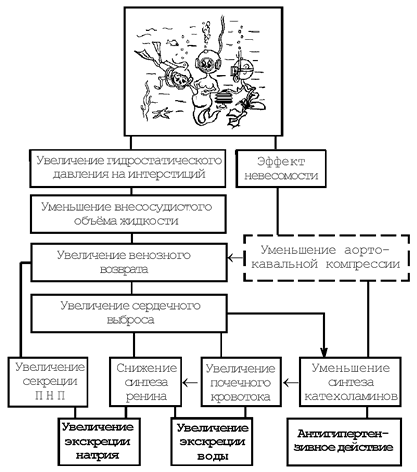
Рис. 25. Механизмы физиологических изменений при водно-иммерсионной компрессии (ВИК).
Погружение в воду вызывает перераспределение крови и увеличение венозного возврата. Четверть века тому назад группа исследователей под руководством M.J.Arborelius [53] показала, что с момента погружения происходит увеличение внутригрудного объёма крови приблизительно на 700 мл и соответствующее увеличение ЦВД с 3 до 15 мм рт.ст. Увеличение количества крови, притекающей к полостям сердца, должно приводить к росту производительности миокарда без включения механизмов ритмоинотропной зависимости. И действительно, в наших исследованиях на II и III этапах отмечалось достоверное увеличение СИ по отношению к исходным показателям. При этом, не наблюдалось увеличение ЧСС, что подтверждает важную роль закона Франка-Старлинга в выявленных изменениях (рис. 26).
Это подтверждается также выявленной корреляционной зависимостью между УО и КДО (r=0,627) и фракцией выброса (r=0,514).
По-видимому, при погружении в воду действует эффект невесомости. Учитывая особенности связочного аппарата матки, можно предположить, что при погружении в воду матка как бы всплывает, устраняя аорто-кавальную компрессиию и увеличивая преднагрузку. Эффективность погружения в воду в отношении синдрома АКК ешё предстоит изучить, тем более, что и законы физики и гидравлики надо бы надёжнее «притереть» к такому феномену. Пока же мы полагаем, что увеличение преднагрузки происходит главным образом за счёт увеличения ОЦК при внешней компрессии отёчных тканей.
Погружение в воду сопровождается увеличением давления в правом предсердии и лёгочной артерии. В наших исследованиях уже ко II этапу отмечается значительный прирост КДО (рис. 27), связанный с увеличением объёма циркулирующей плазмы (r = 0,758).
Цепь последовательно развивающихся эффектов, обспечивает увеличение объёма циркулирующей плазмы.
Ещё в 1963 г. было высказано предположение, что перераспределение крови при погружении в воду связано с внешнем давлением на ткани, которое оказывает столб жидкости [114]. Давление воды на поверхность тела возрастает в зависимости от глубины погружения: на глубине 0,5 м избыточное давление составляет 50 см вод.ст., благодаря чему происходит перераспределение крови и жидкости из периферических тканей к внутренним органам. Проявление этого механизма значительно облегчается при уменьшении АКК, т.к. у беременных в третьем триместре большая часть жидкости секвестрируется в тканях нижних конечностей. Подтверждением этому является снижение тока крови в нижних конечностях во время погружения, а также сравнительный анализ диуреза у здоровых (494±89 мл за 3 часа) и больных с ампутированными конечностями (183±48/3 мл за 3 часа) [251].
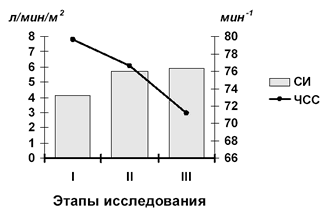
Рис. 26. Изменения ЧСС и СИ в процессе терапии методом ВИК у больных преэклампсией.
Важный механизм действия ВИК – перераспределение жидкости из интерстициального пространства в сосудистое. Подтверждением этого механизма является увеличение ОЦП. Прямое измерение внутритканевого давления во время погружения в воду показывает, что оно превышает внутрисосудистое [186], благодаря чему в просвет сосуда проходит избыточная жидкость из интерстициального пространства.
Водно-иммерсионная компрессия отёчных тканей приводит к увеличению гидростатического давления в интерстиции. Даже при выраженных отёках у беременных гидростатическое давление во внесосудистом пространстве составляет всего 0,7 мм рт.ст. Следовательно, для того, чтобы создать обратный градиент, способный вытолкнуть жидкость из внесосудистого пространства, уже достаточно водного столба высотой, превышающей 1 см (10 мм вод.ст. соответствует 0,735 мм рт.ст.). В этих условиях создавшийся градиент приводит к увеличению резорбционных сил Старлинга в венозной части капилляра и аутотрансфузии жидкости из внесосудистого пространства в сосудистое русло.
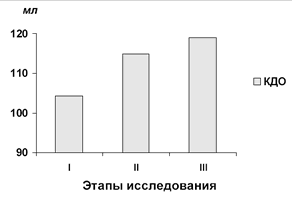
Рис. 27. Изменения КДО левого желудочка при ВИК у больных преэклампсией.
Вероятно, такая аутогемодилюция будет тем большей, чем больше жидкости секвестрировано во внесосудистом пространстве. Мы провели сравнительные исследования увеличения КДО в зависимости от выраженности отёчного синдрома (рис. 28).
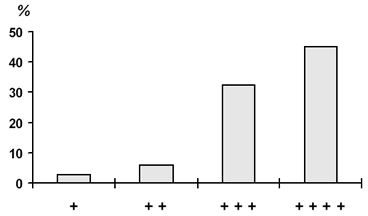
Рис. 28. Зависимость изменений КДО от тяжести отёчного синдрома. Знаками «+» отмечена степень отёчности.
Исходя из анализа полученных результатов, можно заключить, что одним из основных показаний к проведению терапии методом ВИК у беременных с преэклампсией является отёчный синдром. Увеличение ОЦК сопровождается аутогемодилюцией и происходит за счёт увеличения ОЦП жидкостью, ранее секвестрированной во внесосудистом пространстве (рис. 29). Это наглядно иллюстрируется относительным снижением на II и III этапе количества эритроцитов, показателей Гб (на 10,13 и 11,78%), Гт (на 13% и 12,76%), увеличением ОЦП на 15 и 17,29% соответственно, по отношению к исходным показателям.
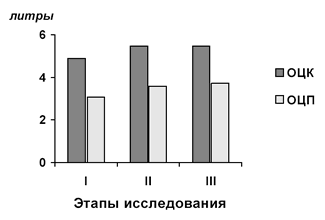
Рис. 29. Изменения ОЦК и ОЦП при ВИК у больных преэклампсией.
Во время погружения в воду уменьшается вязкость крови, что в сочетании со снижением тонуса сосудов микроциркуляции улучшает реологические свойства крови [96].
Возможно, выявленные нами изменения могут быть результатом ещё одного механизма – компрессии сосудов-ёмкостей – мелких периферических венул (15-100 мкм) и выдавливанием их содержимого в кровоток. Существует мнение, что мелкие венулы содержат кровь с более низким гематокритным числом, чем вены более крупного калибра, и это приводит к эффекту гемодилюции.
По-видимому, физиологические эффекты невесомости, которые моделируются при погружении в воду, и сама по себе ВИК не являются единственной причиной выявленных нами гемодинамических и волемических эффектов. Вполне вероятно, что на эти эффекты может оказывать влияние рефлекторный ответ, который зависит от состава жидкости, в которую погружён человек. При изучении гемодинамических эффектов погружения в Мёртвом море (удельный вес воды около 1,19) было обнаружено парадоксальное уменьшение натрийуреза, увеличение систолического, диастолического артериального давления и ОПСС [143].
Вероятно аутогемодилюция, связанная с ВИК, сопровождается обратным поступлением белков, секвестрированных в интерстициальном пространстве. В наших исследованиях, несмотря на значительное увеличение ОЦП и снижение гематокрита, концентрация общего белка в плазме остаётся без изменений, и общая масса циркулирующего белка существенно возрастает (рис. 30).
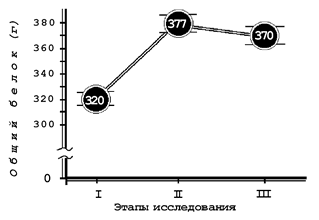
Рис. 30. Изменения общей массы циркулирующего белка при ВИК у больных преэклампсией.
Это противоречит данным, полученным D.G.Bichet e.a., которые отмечают уменьшение концентрации общего белка на фоне гемодилюции [61]. Мы объясняем это противоречие тем, что D.G.Bichet e.a. изучали белки крови при гепато-ренальном синдроме. Полученные нами данные позволяют предположить, что терапия ВИК способна корригировать коллоидно-осмотическую недостаточность плазмы в условиях эндотелиального повреждения. Дальнейшие исследования КОД при погружении в воду у разных контингентов больных позволят проверить это предположение.
Среди прочих благотворных эффектов, которые оказывает ВИК на систему кровообращения, выявлена отчётливая тенденция к уменьшению АГ на фоне снижения потребности в антигипертензивных средствах. Примечательно, что уменьшение артериальной гипертензии происходит параллельно с устранением периферической вазоконстрикции (рис. 31).
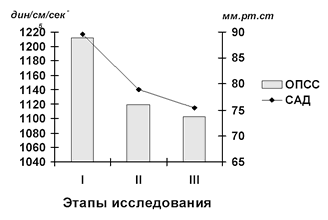
Рис. 31. Изменения САД и ОПСС при терапии ВИК у больных преэклампсией.
Гипотензивный эффект ВИК связан с уменьшением синтеза ренина и активности симпатической нервной системы. Это подтверждается уменьшением концентрации катехоламинов в плазме и их метаболитов в моче [126].
Система дыхания и метаболизм
Мы исследовали показатели механики дыхания, газового состава и кислотно-основного состояния крови у беременных с преэклампсией под влиянием терапии методом ВИК. Исследования проводились до погружения в воду (I этап), спустя час пребывания беременной женщины в воде (II этап) и через три часа после окончания проведения сеанса (III этап). Анализ полученных результатов выявил отрицательное влияние ВИК на параметры механики дыхания.
При нормально развивающейся беременности рост беременной матки поднимает диафрагму, уменьшая внутренний вертикальный размер грудной полости в среднем на 4-5 см. Однако, это не сопровождается уменьшением ЖЕЛ, т.к. подъём диафрагмы уравновешивается увеличением передне-заднего и поперечного диаметров грудной клетки за счёт роста подрёберного угла. Возможно, ВИК нивелирует положительное влияние этих компенсаторных механизмов или действует другой механизм, но уже ко II этапу в наших исследованиях отмечено снижение ЖЕЛ на 11,1%, которая не возвращается к исходным показателям даже спустя три часа постиммерсионного периода (рис. 32).
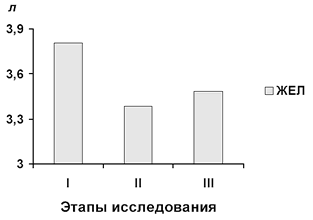
Рис. 32. Изменения ЖЕЛ при ВИК у больных преэклампсией.
Можно выделить по крайней мере три основные причины этих изменений:
- при погружении в воду непосредственно на грудную клетку воздействует окружающее гидростатическое давление, значительно увеличивая работу дыхательных мышц;
- ВИК увеличивает подъём диафрагмы;
- во время пребывания в воде происходит увеличение кровонаполнения лёгких, как следствие общего смещения крови и жидкости из периферических тканей к внутренним органам.
В исследованиях, выполненных на здоровых добровольцах, установлено, что при погружении в воду внутригрудной объём крови увеличивается в среднем на 700 мл [216]. Увеличение кровонаполнения лёгких должно уменьшать их растяжимость и способствовать раннему экспираторному закрытию дыхательных путей, которое характеризуется объёмом закрытия лёгких (ОЗЛ). Увеличение ОЗЛ на фоне исходно сниженной функциональной остаточной емкости лёгких у беременных может приводить к сокращению резерва ФОЕ и связанному с этим нарушению вентиляционно-перфузионных отношений и развитию гипоксии [24]. Этот отрицательный эффект ВИК у беременных ещё предстоит исследовать хотя бы для того, чтобы убедиться в безопасности проведения длительных сеансов терапии и выявить группу риска больных, у которых применение метода может не только не улучшить состояние, но и нанести вред.
Даже при нормально протекающей беременности эластическая тяга лёгочной ткани увеличивается, то есть снижается растяжимость лёгких. При развитии преэклампсии интерстициальная гипергидратация увеличивает жесткость лёгких ещё больше. В наших предыдущих исследованиях, выполненных на базе Перинатального центра Республики Карелия, у больных с лёгкой формой преэклампсии растяжимость системы лёгкие-грудная клетка уменьшалась на 14,04% по сравнению со здоровыми беременными [30]. Возможно, эти же механизмы (отёк и набухание слизистой) в сочетании с увеличением полнокровия лёгких служат причиной выявленного уменьшения проходимости мелких бронхов при погружении в воду. Обнаружено, что во время проведения сеансов ВИК, максимальные объёмные скорости, характеризующие проходимость периферических дыхательных путей снижаются (рис. 33).
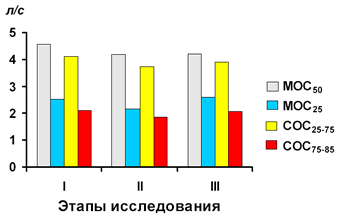
Рис. 33. Проходимость периферических дыхательных путей при ВИК у больных преэклампсией. МОС50, 2b5, 25-75, 75-85 – максимальная и СОС – объёмная скорость выдоха при соответствующем уровне ЖЕЛ (50%, 25% и т.п.).
Исследование изменений КОС при погружении в воду не выявило каких-либо существенных изменений показателей (табл. 3).
ВИК, как и всякая другая методика лечения, не должна быть идеализирована. Несмотря на её многочисленные преимущества перед инфузионной терапией, ВИК, положительно влияя на гемодинамику, способна отрицательно отражаться на внешнем дыхании.
Дальнейшие исследования позволят выявить конкретных больных, у которых этот метод требует специальных мер коррекции дыхательных нарушений или даже противопоказан. Тем не менее, уже сегодня можно сказать, что терапия методом ВИК должна с особой осторожностью применяться у больных с выраженными нарушениями гемодинамики в малом круге кровообращения.
| Изучаемые показатели | Этапы исследования | |
| I | II | |
| pO2, мм рт.ст. | 87,47±1,221 | 78,99±1,947 |
| Sо2, % | 97,16±0,270 | 95,66±0353 |
| pCO2, мм рт.ст. | 32,27±0,848 | 30,71±0,944 |
| pH | 7,407±0,050 | 7,431±0,67 |
| BE, ммоль/л | -3,43±0,425 | -2,28±0414 |
| BEecf, ммоль/л | -4,41±0,455 | -3,36±0,486 |
| BB, ммоль/л | 44,56±0,418 | 45,71±0,418 |
| HCO3–, ммоль/л | 19,38±0,502 | 20,21±0,467 |
с преэклампсией при водно-иммерсионной компрессии (M±m)
Функция почек и метаболизм
Одним из основных эффектов погружения является повышение диуреза. Уже на II этапе наших исследований отмечается отчётливое увеличение темпа диуреза (рис. 34). Это вполне естественный ответ на рост ОЦК и венозного возврата к сердцу. В механизме увеличения экскреции почками натрия и воды, большое внимание уделяется роли барорецепторов низкого давления.
J.P.Henry и O.H.Gauer ещё в 1956 г. предположили существование кардио-ренального рефлекса, опосредованного возбуждением механорецепторов полостей сердца и стимуляцией n.vagus [137]. Этот механизм получил впоследствии название рефлекса Генри-Гауэра.
Почему при водно-иммерсионной компрессии у беременных с преэклампсией наряду с отчётливым диуретическим эффектом отмечается увеличение КДО, гемодилюция и рост ОЦП? Повидимому, ВИК восстанавливает ауторегуляцию, и жидкость, ранее секвестрированная в интерстициальном пространстве, попадает в сосудистое русло. В связи с этим ВИК должна быть особенно эффективной у тех больных, у которых интерстициальная гипергидратация сочетается с гиповолемией. Поскольку у здоровых беременных таких нарушений нет, то использование у них сеансов ВИК в качестве профилактики может оказаться неэффективным или даже, напротив, приводить к гиповолемии, стимулируя избыточный диурез. Этот эффект довольно точно описан при исследовании здоровых добровольцев специалистами аэрокосмической медицины [242]: после первого часа погружения количество мочи увеличивается более чем в три раза, достигая пика на втором часу. Это заставило нас выбрать продолжительность сеансов ВИК у беременных 1,5-2 часа.
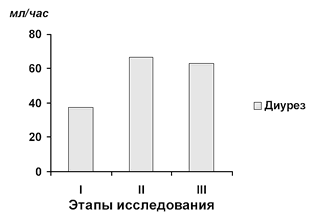
Рис. 34. Изменение диуреза при ВИК у больных преэклампсией.
Диуретический эффект ВИК нельзя сводить к простому механическому воздействию столба жидкости на отёчные ткани. Повидимому, увеличение диуреза и натрийуреза обеспечивают несколько механизмов:
- изменение внутрипочечной гемодинамики, включая уменьшение сопротивления сосудов почек;
- гормональный сдвиг и уменьшение активности симпатической нервной системы;
- уменьшение клубочкового капиллярного давления.
Более 70 лет назад H.C.Bazett в уже упоминавшейся нами работе [59] связал погружение в ванну при термонейтральной температуре с увеличением экскреции натрия. В последующие 60 лет многочисленные исследователи подтвердили связь погружения в воду с ростом натрийуреза. Диуретический эффект ВИК осуществляется в дистальном отделе нефрона, где происходит снижение реабсорбции натрия на фоне увеличения доставки натрия к этому отделу.
Погружение в водную среду комфортной температуры сопровождается не только уменьшением ОПСС, но и рефлекторным расширением сосудов почек [227]. Видимо, этот механизм также способствует диуретическому эффекту.
Гиперволемия приводит к улучшению перфузии всех органов, и в результате улучшения печёночного кровотока значительно увеличивается метаболизм многих гормонов, включая активный ренин плазмы и альдостерон. Снижение активности альдостерона – один из мощных стимулов натрийуреза. Полагают, что первичным звеном, ведущим к снижению уровня альдостерона, является угнетение активности ренина.
Уменьшение выработки ренина и альдостерона подтверждается увеличением натрийуреза, хотя выявленный нами калийурез, сопутствующий натрийурезу, несколько умаляет роль альдостерона (рис. 35).
Подтверждением этому является тот факт, что назначение минералокортикоидов не устраняет натрийурез, вызванный погружением в воду. В наших исследованиях количество натрия, экскретируемого с мочой, увеличивается уже ко II этапу исследования. Некоторые исследователи связывают этот эффект с увеличением синтеза предсердного натрийуретического полипептида (ПНП) в результате увеличения притока крови к правым отделам сердца [199].
Обнаружение ПНП позволило даже называть сердце эндокринной железой. В 1981 г. A.J.Debold e.a., вводя внутривенно неочищенный экстракт предсердия, отметили, что он вызывает значительное увеличение диуреза, экскреции натрия и хлора, а также умеренный калийурез [90]. Потом были выявлены и другие эффекты ПНП – снижение сосудистого тонуса, угнетение биосинтеза адреналина, альдостерона и притока жидкости в интерстиций. Одной из тем исследований, связанных с погружением в воду, стало изучение роли ПНП как фактора, вызывающего натрийурез. Внутрипочечным механизмом действия ПНП является активация им рецепторов, расположенных в медуллярной зоне.
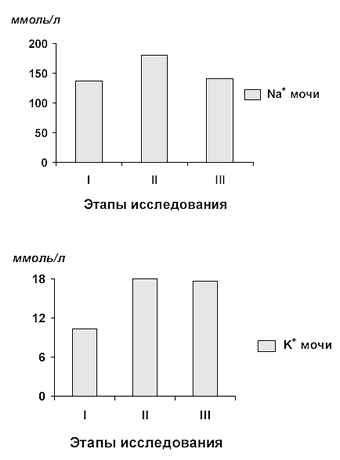
Рис. 35. Экскреция натрия и калия с мочой при ВИК у больных преэклампсией.
Стремление свести толкование диуретического и натрийуретического эффектов ВИК только к работе двух гормональных систем представляется нам излишне упрощенным. Натрийурез может быть отчасти обусловлен увеличением синтеза простагландинов, в частности простогландина Е. Так, назначение индометацина значительно уменьшает натрийуретический эффект у здоровых лиц при погружении в воду [217].
Снижение активности симпатической нервной системы и уровня катехоламинов при ВИК, отмечено большинством исследователей. Оно ведёт к уменьшению сопротивления почечных сосудов и перераспределению почечного кровотока. Повышение кровотока в кортикальной зоне препятствует обратной реабсорбции натрия и воды.
Натрийурез зависит от общего содержания натрия в организме. Низкое содержание натрия уменьшает его экскрецию и, соответственно, диурез. Мы не раз уже подчёркивали вредность традиционной рекомендации исключить поваренную соль из рациона. При этом не только задерживается жидкость, но и снижается чувствительность адренорецепторов гладкомышечных клеток и тромбоцитов к катехоламинам и ангиотензину. По мнению большинства исследователей диуретического эффекта погружения в воду, среднесуточное потребление хлорида натрия должно составлять не менее 3-4 г в день [265].
Наряду с увеличением экскреции натрия нами выявлено увеличение кальцийуреза (рис. 36). Преэклампсия сопровождается развитием гипокальцийурии, которая является очень ранним признаком заболевания и обычно предшествует появлению триады симптомов Цангемейстера, в связи с чем увеличение экскреции кальция с мочой может быть расценено как благоприятный прогностический признак. В наших исследованиях увеличение кальцийурии сопровождалось уменьшением САД (r=0,802) и снижением потребности в антигипертензивных средствах. Кальцийурез не связан с паратиреоидным гормоном или изменениями КОС. Вероятно, что он обусловлен увеличением доставки кальция к почечным канальцам.
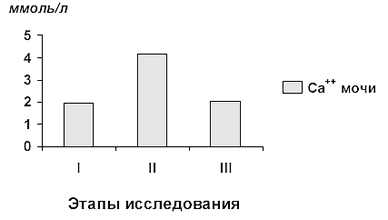
Рис. 36. Кальцийурез при ВИК у больных преэклампсией.
Дегидратационному эффекту подвергается не только интерстициальное пространство, но и, повидимому, сами клетки периферических тканей. Нами отмечено увеличение экскреции калия с мочой без существенных изменений концентрации К+ плазмы. Механизм клеточной дегидратации до конца не ясен, но его существование подтверждается влиянием погружения в воду на ионный состав внутри- и внеклеточной жидкости.
Как известно, почечная экскреция натрия и калия у людей подвержена циркадному ритму с максимальными значениями сразу после полудня и минимальным к полуночи. Стимулируемый ВИК диурез и натрийурез также в значительной степени подвержены циркадным ритмам. Ночной сеанс водной иммерсии намного меньше увеличивает диурез и натрийурез в сравнении с сеансом в утренние часы. Поэтому оптимальным является использование метода в первой половине дня.
Диуретический эффект ВИК зависит и от глубины погружения. Например, погружение в воду до уровня талии не вызывает заметного увеличения экскреции натрия.
Температура воды должна быть в пределах 34-35oС. Только в этих границах метод ВИК приводит к описываемым физиологическим явлениям. Изменение температурного режима ярко проявляется в величине сердечного выброса. При более высокой температуре соответственно возрастает сердечный выброс. При температуре выше 37oС повышение сердечного выброса происходит как за счёт ударного объёма, так и тахикардии, тогда как режим 34-35oС характеризуется увеличением ударного объёма без тахикардии. Снижение ОПСС и сопротивления сосудов почек также зависит от температуры воды. Холодная вода способствует периферической вазоконстрикции, которая соответственно изменяет реакцию системы кровообращения, почек и синтез различных гормонов, регулирующих нормальное взаимодействие этих систем. Наибольшее уменьшение ОПСС наблюдается при погружении в воду термонейтральной температуры [62].
Методика проведения ВИК
Суть метода ВИК состоит в погружении в ванну, заполненную водопроводной водой термонейтральной температуры (34o-35o), до уровня VI шейного позвонка в течение 1,5-2 часов.
Предварительная подготовка. Установить натриевокалиевую диету (Na+ 150 ммоль/сут, K+ 80 ммоль/сут). При меньшем содержании натрия включаются механизмы, способствующие его задержке, и, соответственно, уменьшается темп диуреза.
Непосредственно перед погружением дать больным выпить 200 мл воды. Полагают, что приём жидкости снижает уровень антидиуретического гормона. Если погружение в воду проводится у дегидратированных больных, диуретический эффект значительно снижается.
Опорожнить мочевой пузырь.
Проведение процедуры. Погружение проводить в ванну, наполненную водопроводной водой с температурой 34-350.
Уровень погружения – до VI шейного позвонка, в положении женщины лёжа на спине.
Продолжительность сеанса 1,5-2 ч. в первой половине дня, проводятся ежедневно.
При анализе наших результатов не выявлено достоверного различия между III и II этапами исследования. Более того, после 5-7 погружений отмечается уменьшение клинической эффективности метода (динамики веса, темпа диуреза, экскреции электролитов, уменьшения степени отёчности и т.д.). Это позволяет определить эффективный курс проводимой терапии как 5-7 погружений, что вполне перекликается с рекомендациями пророка Елисея, приведёнными в Ветхом Завете Библии.
«Пойди, омойся семь раз в Иордане и обновится тело твоё у тебя, и будешь чист!» (4 Цар, 5, 10). Так и случилось, хотя Елисей лечил не преэклампсию беременных, а проказу у Неемана, военоначальника Сирийского царя, но подкупает простота метода, тем более, что проказу и сегодня вылечить достаточно сложно. А преэклампсию – легко?
Несмотря на длительность предшествующего течения преэклампсии, перинатальной смертности в нашем материале не отмечено ни в одном случае, тогда как в группе беременных с преэклампсией, которым проводилась традиционная инфузионная терапия, перинатальная смертность составила 9,3‰. Проводимый биомониторный контроль при использовании ВИК выявил улучшение состояния плода. Частота операции кесарева сечения составила 8,94%, причём ни в одном случае оперативное родоразрешение не проводилось по показаниям, связанным с тяжестью преэклампсии.
Метод ВИК оказался эффективным у 83,4% больных, что позволило пролонгировать беременность до 37-39 недель, периодически повторяя курсы терапии по мере нарастания симптоматики. На фоне проводимой ВИК отмечено клиническое улучшение течения заболевания, уменьшение степени отёчности, улучшение микроциркуляции, регресс неврологической симптоматики, оптимизация темпа диуреза, уменьшение и стабилизация массы тела. Во время лечения количество экскретируемой жидкости превышало выпитую на 300-400 мл.
Результаты наших исследований и клинических наблюдений ещё не позволяют дать исчерпывающий ответ на многие вопросы, касающиеся конкретных механизмов действия водно-иммерсионной компрессии. Тем не менее, в сравнении с общепринятыми методами коррекции гиповолемии у больных преэклампсией, метод ВИК представляется более физиологичным и безопасным, поскольку направлен на восстановление ауторегуляции функций. В такой ситуации увеличение ОЦК и регионарное распределение сердечного выброса контролируется волюм-рецепторами сосудов и барорецепторами правого сердца. При сохранённой экскреторной функции почек организм сам решает, какой объём внутрисосудистой жидкости является избыточным, и выводит его. И зависит это не от инструкций и даже не от знаний врача, назначающего тот или иной объём инфузионной терапии или диуретик, а от восстановленных механизмов ауторегуляции.


