Respiratory disorders
Нарушения дыхания (Часть 4)
Malcolm I. Levene, David I. Tudehope, M. John Thearle
Главы из книги "Essencials of Neonatal Medicine"
Гиполазия легких (недоразвитость легких)
Для адекватного развития легких плод должен иметь возможность совершать дыхательные движения и перемещать столб амниотической жидкости вверх и вниз по трахее и главным бронхам. Следовательно, гиполазия может возникать по следующим причинам:
- недостаточность дыхания плода (нейромышечные расстройства);
- невозможность расширять легкие (диафрагмальная грыжа, плевральный выпот);
- недостаток ликвора (маловодие) из-за почечных нарушений или нарушений шейки мочевого пузыря или продолжительной пункции околоплодного пузыря.
Младенцы с гипоплазией легких могут одновременно иметь нарушения лица и контратуры конечностей. Плацента со стороны плода должна быть внимательно исследована на amnion nodosum , который предполагает тяжелое маловодие, главным образом, синдром Поттера.
Клинические признаки
У младенцев с самого рождения развивается тяжелый респираторный дистресс с заметной гипоксией, гиперкапнией и метаболическим ацидозом. Частым осложнением является пневмоторакс. Легкие очень жесткие и движения грудной клетки очень маленькие при искусственной вентиляции. На рентгене грудной клетки диагностика гипоплазии легких может быть затруднена. Тяжелая гипоплазия легких несовместима с жизнью, а менее тяжелые формы вносят свой вклад в хроническую зависимость от вентилятора и бронхо-легочную дисплазию.
Массированное легочное кровотечение
Массированное легочное кровотечение у новорожденных имеет характерное клиническое проявление в форме сердечно-сосудистого коллапса, и связанного с ним излития из трахеи и рта окрашенной кровью жидкости. Состояние обычно фатально и встречается приблизительно в 1 случае на 1000 родов. Оно описано в связи с тяжелой родовой асфиксией, гипотермией, маленьким сроком беременности при рождении ребенка, расстройствами коагуляции и конгенитальным сердечным заболеванием. Сообщалось о легочном кровотечении, последовавшем после терапии экзогенным сурфактантом. В большинстве случаев вероятной причиной предполагался геморрагический отек легких.
Лечение
Лечение такое же, как при респираторном дистрессе (см. след. пуьликации). Однако особенное ударение необходимо сделать на следующем:
- реанимация сердечно-сосудистого коллапса восполнителями объема, такими как белки плазмы;
- лечение отека легких фруземидом и, возможно, морфином
- коррекция расстройств свертываемости крови
- если необходима искусственная вентиляция, для снижения кровотечения следует применять высокое ПДКВ.
Конгенитальная диафрагмальная грыжа
Обычно грыжа бывает заднелатерального типа ( Bochdalek ); 80% встречаются с левой стороны. Она образуется через дефект в диафрагме в результате устойчивого плевроперитонеального канала, обусловленного недостаточностью компонентов мускулатуры. Благодаря дефекту в диафрагме абдоминальные структуры проникают в грудную клетку, обуславливая образование грыжи. Затем происходит гипоплазия или компрессия легкого на стороне грыжи со смещением средостения к контрлатеральной стороне. Иногда имеет место гипоплазия контрлатерального легкого. Младенцы с большой диафрагмальной грыжей имеют после рождения быстро прогрессирующую дыхательную недостаточность с устойчивым цианозом. Менее острая диафрагмальная грыжа может проявиться уже в детском отделении, и сопровождаться респираторным дистрессом. Также при рутинном исследовании случайно может быть обнаружена ‘декстрокардия' или ладьевидный живот. На аускультации легких, звуки живота могут быть слышны на пораженной стороне, если газ проникает в желудочно-кишечный тракт. При нормальном давлении легкие не будут адекватно раздуваться.
Диагноз
Большинство случаев сейчас диагностируются внутриутробно рутинным акушерским УЗИ при 17-19 неделях беременности или последующим исследованием на многоводие. Диагноз диафрагмальной грыжи подтверждается рентгеном грудной клетки. На таком рентгеновском снимке виден кишечник, заворачивающийся петлей в грудную клетку (рис. 10.9).
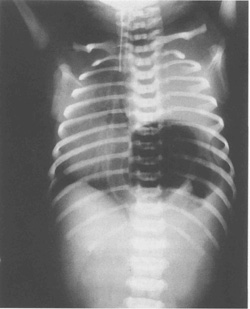 |
| Рис. 10.9. Рентген грудной клетки показывает левостороннюю диафрагмальную грыжу |
Если рентген сделан вскоре после рождения, возможно, будет затруднительно определить, находится ли кишечник в грудной клетке, особенно если в желудочно-кишечном тракте немного воздуха. Рентген должен проводится с рентгеноконтрастным катетером в желудке и должен включать брюшную полость, чтобы показать малое количество абдоминального газа. Более редкая форма диафрагмальной грыжи развивается через антеромедиальный дефект, ниже грудины (тип Morgagni ). В этом случае она обычно содержит часть толстой кишки. Как правило, симптоматика при этом отсутствует, и патология часто обнаруживается на латеральном рентгене грудной клетки.
Лечение
Если имеются подозрения на конгенитальную диафрагмальную грыжу, должен быть введен желудочный зонд (orogastric tube), и абдоминальная составляющая, находящаяся в грудной клетке, аспирируется, свободная от газа и секреции. Если ребенку требуется вспомогательная вентиляция, то она должна проводиться через эндотрахеальную трубку и никогда – с помощью мешка или маски, поскольку это может увеличивать растяжение кишечника внутри грудной клетки. Должны предприниматься меры по предотвращению разрыва контрлатерального легкого, поскольку жизнь ребенка почти исключительно зависит от вентиляции этого легкого. В соответствии с первичным диагнозом, необходимо стабилизировать состояние ребенка и вызвать детского хирурга для оперативного лечения. В более тяжелых случаях хирургическое вмешательство часто откладывается на 3-7 дней для обеспечения максимальной стабилизации состояния младенца, часто с помощью высокочастотной осциляторной вентиляции. Операция состоит из редукции абдоминальной составляющей, закрытия диафрагмального дефекта и коррекции любой мальротации кишечника.
Легочная гипертензия является обычным осложнением тяжелой диафрагмальной грыжи и, как правило, развивается вслед за послеоперационным «медовым» периодом, равным 24-48 часов. На третьи сутки у младенца развивается тяжелая гипоксия с право-левым шунтом. Для уменьшения риска осложнений рекомендуется плановая гипервентиляция, а для снижения алкалоза (рН<7.5) - инфузия бикарбоната натрия. Сульфат магния, простоциклин или толазолин может иметь значение, но вдыхаемая закись азота не имеет длительного благоприятного воздействия (см. стр. 200). В более тяжелых случаях может быть необходимым продолжение послеоперационной анестезии с параличом мышц на момент возвращения из операционной. Экстракорпоральная мембранная оксигенация имеет минимальную пользу в этом состоянии.
Прогноз
Прогноз зависит от степени легочной дисплазии и времени проявления патологии. Младенцы с респираторным дистрессом в первые 6 часов имеют высокую смертность (около 70%) , для тех, у кого она проявилась между 6 и 24 часами прогноз намного лучше (уровень смертности 10-15%). Маловероятно, что более позднее проявление респираторного дистресса связано с легочной дисплазией, и в этом случае прогноз очень благоприятный. Признаки неблагоприятного прогноза включают многоводие, устойчивый повышенный уровень РСО2 при среднем давлении в дыхательных путях > 20 см вод. ст. и гипоксия, требующая легочных вазодилатоторов.
Эзофагеальная атрезия и трахеоэзофагеальная фистула
Эзофагеальная атрезия является конгенитальной аномалией, при которой обычно полностью перекрыт просвет пищевода, в результате чего пищевод имеет форму слепого верхнего кармана. Это часто связано трахеоэзофагеальной фистулой. Наиболее часто встречаются случаи, когда верхняя часть пищевода заканчивается слепым концом (верхний эзофагеальный карман), а его нижняя часть поднимается из трахеи, выше ее киля (рис. 10.10с). Другие варианты встречается намного реже.
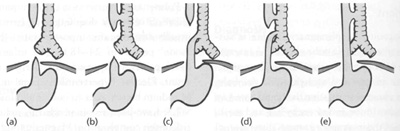 |
| Рис. 10.10. Варианты трахео-эзофагеальной фистулы с или без эзофагеальной атрезией. Тип С ответственен за 85% случаев, остальные типы в равной степени редки. |
Клинические признаки
Многоводие у матери встречается в 60% случаев и в огромной степени ответственно за высокую частоту преждевременных рождений. Эзофагеальная атрезия связана с избыточной продукцией слюны и слизи, а также с высокой частотой аспирационной пневмонии. Если младенец накормлен, молоко аккумулируется в верхнем кармане и сливается в трахею. Аспирация желудочного содержимого и желчи в бронхиальное дерево приводит к легочным осложнениям с коллапсом и пневмонией. Абдоминальное растяжение происходит из-за прохождения воздуха вниз через фистулу в желудок и может развиваться очень быстро.
Возможно наличие сосуществующих конгенитальных аномалий, и они могут быть большими или незначительными. Большие аномалии включают заболевания сердца, интерстициальную атрезию, неперфорированный анус (атрезия заднего прохода) и аномалии почек. VACTERL -связь является термином, часто используемым для описания аномалий. Эта аббревиатура состоит из следующих слов : Vertebral (Позвоночный), Anal (Анальный), Cardiac (Сердечный), Tracheal (Трахеальный), 'Esophagus' (Пищеводный), Renal (Почечный) и Limb (Относящийся к конечностям). Наиболее важным аспектом эзофагеальной атрезии является то, что она должна быть распознана как можно скорее после рождения, предпочтительно до первого кормления, так чтобы свети к минимуму вероятность возникновения легочных осложнений. Каждому ребенку должна вводиться назогастральная трубка размером 5 через каждую ноздрю вниз в желудок вскоре после рождения. Этим методом еще до кормления может быть обнаружено большинство случаев эзофагеальной атрезии и хоанальной атрезии. Если это не практикуется, эзофагеальная атрезия в общем случае может быть распознана по избыточной секреции или цианозу и кашлю, сопровождающему кормления. Точный диагноз определяется в том случае, если невозможно провести твердый рентгеноконтрастный катетер номер 10 в желудок в связи с тем, что он задерживается на расстоянии примерно 10 см от уровня губ. Как только катетер прошел настолько далеко, насколько возможно, должен быть проведен рентген шеи и верхней части груди для подтверждения того, что он был заблокирован из-за непроходимости на этом уровне. Ренген абдоминальной области должен проинспектировать желудок на наличие газа, а с помощью ренгена грудной клетки можно оценить области спадения (коллапса). Воздух является хорошей контрастной средой в верхнем кармане. Обычно нет необходимости вводить рентгеноконтрастную среду в верхний карман для подтверждения диагноза, но если это сделано, необходимо использовать нераздражающее вещество, такое как метризимид. Для фистулы Н-типа, которая проявляется рецидивирующей аспирацией или инфекциями, радиологический диагноз может быть затруднен. Киноконтрастный глоток обычно может подтвердить диагноз.
Лечение
Младенец с эзофагеальной атрезией и трахеоэзофагеальной фистулой должен получать уход, находясь в положении лежа на спине и с приподнятым на 60° головным концом для того, чтобы избежать стекания желудочного содержимого в легкие через фистулу. Должна быть начата внутривенная инфузия и коррекция электролитов и глюкозы крови ребенка для подготовки его к операции. Операция должна проводиться детским хирургом как только ребенок адекватно реанимирован и его состояние стабилизировано. Если имеет место значительная аспирационная пневмония, то потребуются антибиотики. Операция включает разделение трахеоэзофагеальной фистулы и по возможности анастомоз двух сегментов пищевода. Иногда атретический сегмент является слишком длинным, чтобы позволить наложить первичный анастомоз, поэтому требуется эксплантация (выворачивание наружу) цервикальной части пищевода, как эзофагостомия, и желудка, как гастростомия. Определяющая операция должна проводиться в более поздние сроки.
Ребенка с цервикальной эзофагостомией необходимо стимулировать к практике сосания плацебо при одновременном гатростомическом кормлении. Часто возникают осложнения и последствия хирургического вмешательства , которые включают громкий кашель с металлическим оттенком, связанный с сосуществующей трахеомалацией, эзофагеальный стеноз, нарушение анастомоза из-за медиастинита, рецидив трахеоэзофагеальной фистулы и гастроэзофагеальный рефлюкс.
Долевая эмфизема
Конгенитальная долевая эмфизема является редкой аномалией, развивающейся из-за хрящевого дефицита долевого бронха. Эта патология наиболее часто поражает левую верхнюю долю (50%), правую среднюю долю (24%) или правую верхнюю долю (18%), и часто связана с конгенитальным заболеванием сердца (30%), таким как тетралогия Фаллота, заболевание вентрикулярной перегородки или полная аномалия венозного дренажа легких. Развитие респираторного дистресса часто происходит скрыто и незаметно, обычно в течении 2-3 недель и обусловлено коллапсом легких вокруг перераздутой доли. Средостение смещается и стенка грудной клетки выпирает над пораженной областью. Звуки дыхания ослаблены и тоны перкуссии становятся гиперрезонантными. Как только поставлен точный диагноз, в общем случае требуется лобэктомия. Приобретенная долевая эмфизема может быть вторичной по отношению к внешней или внутренней бронхиальной обструкции такой, как закупорка слизью. Этот тип эмфиземы должен лечиться консервативно физиотерапией и постуральным дренажем.
Кистозный аденоматоидный порок развития
Кистозный адемотоидный порок развития (КАПР) является редким кистозным повреждением, более часто встречающимся у мальчиков и часто обнаруживаемым на УЗИ в антенатальном периоде. Это гематомное повреждение может быть связано с многоводием, водянкой плода, преждевременными родами и мертворождением. Имеется три различных типа. Тип I КАПР (70%) представляет собой единичную или множественные кисты, заключенные в одной доле; Тип II КАПР (18%) состоит из множественных кист среднего размера, при этом в 50% таких случаев наблюдаются и другие аномалии; Тип III КАПР (10%) представляет собой грубые повреждения с равномерно распределенными небольшими кистами. Это одно из редких состояний, которое в отдельных случаях лечится хирургией плода.
Хронические легочные заболевание у новорожденных
Хроническое неонатальное заболевание легких обычно определяется как возникающее у преждевременно рожденных младенцев с признаками паренхимального заболевания легких на радиографии грудной клетки, которым требуется увеличение подачи кислорода во вдыхаемой смеси в течение более, чем 28 дней, для поддержания напряжения кислорода >60 мм рт.ст. Sherman et al .(1988) предположил, что для младенцев с очень низким весом при рождении (ОНВР) необходимость в кислороде свыше 36 недель постменструального периода матери является лучшим прогностическим признаком будущих легочных нарушений, чем потребность в кислороде свыше 28 дней с момента рождения.
Классификация различных типов хронического неонатального заболевания легких запутанна. Имеются отдельные единицы, такие как бронхолегочная дисплазия (БЛД), но многие описанные разновидности перекрываются, а у некоторых недоношенных младенцев представлены такие легочные изменения, которые не укладываются ни в одну описанную схему. В таблице 10.4 перечислена классификация хронического неонатального заболевания легких.
Таблица 10.4. Классификация
хронических легочных заболеваний новорожденных
| Бронхолегочная дисплазия |
| Синдром Вильсона-Микити |
| Хроническая легочная недостаточность новорожденных |
Рекуррентная аспирация:Фарингеальная несогласованность |
Интерстициальные пневмонии:Цитомегаловирус |
| Хронический отек легких из-за лево-правого шунта |
| Рахит недоношенных |
Раньше хроническое неонатальное заболевание легких было редким явлением, но с увеличением частоты выживаемости среди чрезвычайно недоношенных младенцев это состояние становится более частым. Приблизительно 80% младенцев с весом при рождении от 501 до 750 г являются зависимыми от кислорода на 28 день; это же касается 40% младенцев с весом при рождении 751-1000 г; и 13% для тех, кто весит 1001-1500 г.
Бронхолегочная дисплазия
Это состояние обычно связано с фазой излечения (выздоровления) от тяжелого РДС, но иногда осложняет аспирацию мекония, легочное кровотечение, тяжелую неонатальную пневмонию или даже рецидивирующее апноэ. Это состояние также называется respirator lung , oxygen - toxic lung (легкое, поврежденное токсическим воздействием кислорода) и болезнь Нортвэя ( Northway et al. 1967).
ЭТИОЛОГИЯ
БЛД возникает у 5% младенцев с очень низким весом и имеет многочисленные этиологические факторы. Частота связана с тяжестью РДС и степенью недоношенности. Это состояние описано только у младенцев, которые получали вентиляцию положительным давлением (этот термин используется для включения давления вдоха, давления выдоха, соотношения вдоха/выдоха и частоты) и имели объемную травму на легком. Напряжение вдыхаемого кислорода более 60% в течение длительного периода времени оказывается необходимым условием развития этого состояния, но не является его причиной. Другими вероятными факторам являются интерстициальная эмфизема и отек легких. Роль гастро-эзофагеального рефлюкса с рецидивирующей аспирацией и инфекционных агентов, таких как Ureaplasma urealyticum , не выяснена.
КЛИНИЧЕСКИЕ ПРИЗНАКИ
Младенцы, у которых развилась БЛД, имеют устойчивое западение грудной клетки, крепитацию (хруст, выявляемый при пальпации) и хрип при аускультации грудной клетки, также наблюдается сильное перераздутие легких и увеличение передне-заднего диаметра грудной клетки. У большинства этих младенцев также имеет место открытый артериальный проток, и через некоторое время может развиться право-сердечная недостаточность ( corpulmonale ).
РАДИОЛОГИЯ
Оригинальное описание БЛД Northway et al . установило радиологическую картину четырех степеней (Таблица 10.5).
Таблица 10.5, Рентгенологическая классификация бронхолегочной дисплазии.
| Стадия | Дни жизни | Описание | Вид на ренгеновском исследовании |
| 1 | 2-3 | Острый РДС | Генерализованная гранулоретикулярная структура, бронхограммы воздуха или "white out" |
| 2 | 4-10 | Период регенерации | Почти полное или полное затемнение |
| 3 | 10-20 | Переходный период | Небольшие кистозные инфильтраты, хроническое заболевание |
| 4 | > 4 недель | Период хронического заболевания | Гиперяркость, длинные инфильтраты наподобие нитки бус, увеличение кист. |
Первые две неотличимы от РДС и не могут служить целям описания. При большинстве тяжелых форм имеется сотовидный (пористый) вид легкого с перераздутыми легочными областями, выраженный фиброз и множественные кисты нерегулярного размера (рис. 10.11). У большинства младенцев с БЛД эти макропризнаки не развиваются, но имеют место более благоприятные, более гомогенные модели нарушений с полосками уплотнений на рентгене грудной клетки.
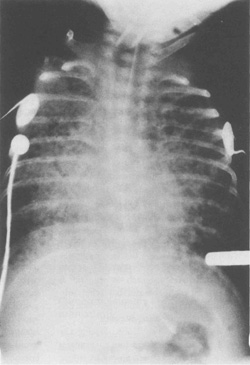 |
| Рис. 10.11. Ренген грудной клетки показывает тяжелую бронхо-легочную дисплазию. |
ЛЕЧЕНИЕ
Предотвращение БЛД требует внимательного ведения младенцев, находящихся на искусственной вентиляции. Легочная интерстициальная эмфизема, отек легких и открытый артериальный проток, а также избыток жидкости увеличивают риск развития БЛД. Описано быстрое закрытие препаратом индометацина, или хирургическим путем открытого артериального протока, что обуславливает застойную сердечную недостаточность. Установленная БЛД часто связана с застойной сердечной недостаточность или cor pulmonale и при этих условиях вводится ограничение жидкости, диуретиков и дигиталиса (или наперстянки). Предполагаются полезными следующие методы лечения:
1 дексаметазон . Исследования показали, что дексаметазон снижает потребность в кислороде у младенцев с БЛД. Курс этого препарата варьирует между 5 и 42 днями, но оптимальная продолжительность и время начала курса не выяснены;
2 диуретики . Терапия диуретиками уменьшает интерстициальную жидкость легких, и было показано, что снижает потребность в кислороде;
3 терапия, направленная на снижение кислородной токсичности . Антиоксиданты, такие как витамин Е оказываются бесполезными, но другие вещества, такие как витамин А и супероксид дисмутаза, в настоящее время оцениваются (исследуются).
4 вентиляция отрицательным давлением . Помещение младенца в резервуар, который обеспечивает прерывистое отрицательное грудное давление, позволяет снизить потребность в кислороде, но этот метод пока не оценен всесторонне, как надежный метод терапии;
Адекватная оксигенация на протяжении всей дневной активности (насыщение О2 92-96%) минимизирует прогрессирование заболевания легочных сосудов. Для обеспечения оптимального роста при наличии высокого энергетического потребления, обусловленного работой дыхания, необходимо удовлетворение дополнительных нутриционных потребностей.
ПРОГНОЗ
Цифры смертности варьируют от 0 до 75 % в зависимости от того, когда был поставлен диагноз. Если диагностирована 4 стадия БЛД в то время, как младенцу по-прежнему требуется вентиляция, шанс отлучить его или ее от вентилятора маловероятен. Большинство младенцев с вылеченной БЛД имеют эпизоды одышки, часто связанные с вирусной инфекцией. Стадия выздоровления связана с продолжительным ростом легких и может занять 2-3 года. Большинство выживших младенцев не проявляют симптомов в течении 2 лет и их рентген грудной кленки остается в норме в течении 2-3 лет. Исследования функции дыхания остаются нарушенными в течение многих лет, хотя у ребенка нет никаких симптомов. Многие младенцы с тяжелой БЛД выписываются домой на непрерывной интраназальной подаче кислорода с небольшой (низкой) скоростью и с периодическим мониторингом потребности кислорода путем пульсоксиметрии.
Было показано, что дети с БЛД имеют повышенное сопротивление дыхательных путей и более подвержены тяжелому дыханию и одышке. Они также имеют повышенную реактивность дыхательных путей. Эпизоды одышки обычно наблюдаются у младенцев и детей, которые имели БЛД в период новорождения. Одышка может быть устойчива к симптомомиметику и ксантину, но стероиды могут быть эффективны.
Инфекция нижних дыхательных путей в первый год жизни имеет особенный риск для детей, которые имели БЛД в неонатальной периоде. У них наиболее вероятно развитие RSV -положительного бронхиолита, который обуславливает наиболее тяжелую дыхательную недостаточность. Антивирусный агент рибавирон (Респигам) и анти- RSV g- глобулин являются эффективными профилактическими агентами. Родителям можно посоветовать стараться не подвергать ребенка риску вирусной инфекции в первый год-два жизни.
Синдром Вильсона-Микити (нарушение созревания легких) ( Northway et al . 1967)
Это состояние возникает у недоношенных детей, рожденных при менее чем 32 неделях беременности и не имеющих РДС. Патология развивается незаметно, в большинстве случаев в течении 2-3 недель и прогрессирует с увеличивающимся диспноэ, ретракцией грудной клетки и увеличением потребности в кислороде.
Первоначально рентген грудной клетки в норме, но билатеральные крупные полосатые инфильтраты с небольшими кистами начинают появляться на второй и третьей неделе. Кисты увеличиваются, и легкие становятся перераздутыми. Остеопения костей и иногда переломы ребер видны на рентгене.
ЭТИОЛОГИЯ
Этиология этого состояния у недоношенных детей неизвестна и может быть обусловлена различными инсультами, включая вирусы, хроническую аспирация молока и задержку бронхиальной секреции. Имеет место увеличивающееся нарушение распределения воздуха с дисбалансом V / Q . Частота заболевания снижается в течение последних десяти лет в то время, как частота БЛД увеличивается. Возможно, что снижение частоты синдрома Вильсона-Микити связано с увеличением использования производных ксантина для предотвращения рецидивирующего апноэ недоношенных.
РАДИОЛОГИЯ
Видны диффузные билатеральные тени, формирующие однообразную похожую на кружева картину с множественными небольшими кистами через оба легочных поля (рис. 10.12).
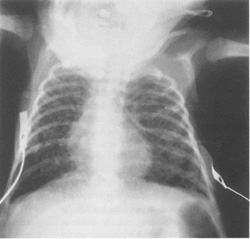 |
| Рис. 10.12. На рентгене грудной клетки при синдроме Вильсона-Микити видно тонкая сеточка. |
ПРОГНОЗ
Большинства младенцев выживают и обычно достигают полного клинического и радиологического выздоровления. Пострадавшим детям может потребоваться дополнительный кислород в течение месяцев прежде, чем заболевание полностью пройдет. Выжившие дети склонны к рецидивирующим эпизодам одышки, связанным с вирусной инфекцией в первые два года жизни.
Хроническая легочная недостаточность недоношенных
Это клиническое состояние обусловлено рядом патологических процессов. Под хронической легочной недостаточностью новорожденных (ХЛНН) понимают ситуацию, когда недоношенному младенцу постоянно требуется кислород или у него развивается потребность в дополнительном кислороде, кроме того, на рентгене грудной клетки у таких младенцев имеется типичная затемненная (подернутая дымкой) картина. Обычно это состояние обусловлено микроателектазами, связанными с жесткими легкими (медленно проходящий РДС), диафрагмальной слабостью или гибкой стенкой грудной клетки. Наиболее частой причиной является поздний неонатальный рахит (см. след. публикации). Недостаточное окостенение ребер совместно с определенной степенью мышечной слабости позволяет легким прогрессивно спадаться. Вирусная инфекция может обусловить такую же картину.
ЛЕЧЕНИЕ
Лечение включает распознавание и лечение рахита, если он имеет место. Для улучшения тонуса мышц могут быть эффективны ксантины, а короткий курс НПДДП применяется для раздувания спавшихся альвеол. Младенцу может потребоваться дополнительный кислород на протяжении несколько недель, но, в конечном счете, он полностью выздоравливает.

