Doppler velocimetry of maternal renal circulation in pregnancy-induced hypertension
Изменение скорости кровотока в системе почечных сосудов на фоне гипертензии, индуцированной беременностью
Hidehiko Miyake, MD, Akihito Nakai, MD, Tatsuo Koshino, MD, Tsutomu Araki, MD
Department of Obstetrics and Gynecology, Tama Nagayama Hospital, Nippon Medical School, 1-7-1 Nagayama, Tama-shi, Tokyo 206-8512, Japan
Статья опубликована в журнале Journal of clinical ultrasound vol. 28, no. 8, October 2001
Абстракт
Цель. Целью исследование было определить, влияет ли гипертензия, индуцированная беременностью (pregnancy-induced hypertension – PIH), на Допплеровские показатели почечного сегментарного и междолевого кровотока по сравнению со здоровыми беременными.
Методы. Волны кровотока в основных почечных, сегментарных и междолевых артериях определялись у 42 здоровых беременных между 24 и 41 неделями беременности, и у 21 женщины с PIH между 28 и 40 неделями беременности. Исследование проводилось с использованием пульсовой Допплеровской сонографии. Авторы использовали спектральный анализ для определения пика систолической и конечно-диастолической скорости кровотока и времени ускорения. Наличие или отсутствие нормальной ранней систолической пластичности комплекса пик-отражение-волна (ESP) оценивалось только в главной почечной артерии.
Результаты. Время ускорения сегментарных и междолевых артерий было значительно дольше в группе PIH по сравнению со здоровыми беременными. У 3 из 21 беременной с PIH наблюдалась потеря ESP в почечной артерии, но данные изменения не были значительными.
Заключения. Снижение систолического ускорения и отсутствие ESP, гемодинамические показатели значительного проксимального стеноза указывают на тяжелый стеноз или продолжительный спазм сосудов в проксимальных артериях, таких как главная почечная или сегментарная артерии. Это может являться частью патогенеза PIH.
Ключевые слова: acceleration time; Doppler ultrasonography; pregnancy-induced hypertension; renal circulation
Гипертензия развивается во время беременности у 4-8% первородящих женщин. Гипертензивные нарушения, осложняющие течение беременности, связаны с повышением уровня заболеваемости и смертности. Несмотря на улучшение акушерского ухода, данные нарушения являются второй причиной материнской смертности (1). Уровень перинатальной смертности также повышается вследствие плацентарной недостаточности, преждевременных родов и отслойки плаценты.
Патологическое состояние почечных сосудов при PIH связано с клубочковым капиллярным эндотелиозом (2). Сокращенное сосудистое ложе почки при PIH уменьшает ток плазмы в почке и скорость клубочковой фильтрации (2). Было выполнено несколько анализов Допплеровского исследования почечного кровотока у здоровых беременных (3-5) и пациенток с PIH (6-9), но разница в показателях между 2 группами была противоречива.
Гемодинамически значимый артериальный стеноз приводит к изменению волн скорости кровотока, которые могут быть диагностированы с помощью Допплеровской сонографии дистальных смежных артерий. Kotval (10) описал подобные изменения в периферических артериях и назвал их волны tardus-parvus. В зоне после стеноза данный феномен проявляется в виде продолжительного времени ускорения, снижения ранней систолической эластичности комплекса пик-отражение-волна (ESP) (10). Было высказано предположение о пользе данного индекса при оценке значительного проксимального стеноза в почечном кровотоке и в случае отторжения трансплантата (11, 12). Nakai и коллеги указали на продолжительное время ускорения и снижение систолического ускорения в междолевых артериях у женщин с PIH. Результаты показывают, что тяжелый стеноз или длительный спазм проксимальных артерий является частью патогенеза PIH.
В ходе настоящего исследования оценивались изменения Допплеровских волн основных почечных, сегментарных и междолевых артерий у пациенток с PIH.
Пациенты и методы
В период с августа 1999 по март 2000 авторы оценили изменения Допплеровской волны скорости кровотока в почечных артериях с двух сторон у 47 беременных без PIH в период с 24 до 41 недели гестации и 21 беременную с PIH при сроке беременности 28-40 недель. Пациентки без PIH были случайно отобраны в условиях женской консультации. Пять пациенток без PIH были исключены из исследования вследствие существующих проблем с почками, включая выраженный гидронефроз или подковообразную почку. Однако мы не исключили пациенток при наличии технических проблем, например отсутствие визуализации почечных артерий. Пациентки включались в исследование, только если PIH была диагностирована менее недели назад и пациентка не успела начать гипотензивную терапию. Никто из пациенток, которые принимали участие в исследовании, не имели болезни почек или эссенциальной гипертензии в анамнезе. Все пациентки подписали письменное согласие на участие в исследовании, которое было одобрено комитетом института.
Согласно определению, PIH – это повыше АД выше 140/90 мм рт. ст. или повышение систолического АД (более 30%) или диастолического АД (более 15 мм рт. ст.) от базального уровня до 16 недель беременности при наличии, как минимум, двух измерений с разницей в 6 часов.
Сонография выполнялась с использованием ультразвукового сканера EUB-555 (Hitachi, Tokyo, Japan). Каждую пациентку осматривали в положении лежа на боку. Вначале выполнялся общий скрининг для исключения выраженных аномалий формы, размера и эхогенности почек. Затем проводилось исследование почек в продольном срезе. Ход основной почечной артерии и ее ветвей, сегментарных и междолевых артерий определялся с помощью цветного Допплера. Волны скорости кровотока определялись в каждой почке. Объем Допплеровской системы был установлен на 3 мм, а фильтр в 100 Hz использовался для снижения шума пульсирующей стенки артерии. Пульсовые волны отражались со скоростью 40-80 мм/секунду. Все исследования проводились одним специалистом.
Спектральный анализ в основной почечной артерии, сегментарной и внутридолевой артериях заключался в определении систолического и конечно-диастолического изменения скорости кровотока и времени ускорения. Наличие или отсутствие нормального комплекса ESP определялось только в основной артерии, так как в других исследуемых артериях данных комплекс чаще всего отсутствует у беременных (7, 13). Как минимум, 3 волны записывались за 1 раз, и наиболее четкое значение выбиралось для анализа. Пиковые систолические и диастолические скорости кровотока определялись на вершине высочайшего систолического пика и в конец диастолы, соответственно. Время ускорения определялось от начала систолического движения до высочайшего систолического пика волны. Любой перерыв в систолическом движении до достижения пика игнорировался. Систолическое ускорение определялось путем деления пикового систолического изменения скорости кровотока в один интервал на время ускорения. Индекс сопротивления (resistance index – RI) рассчитывается следующим образом: (пиковая систолическая скорость кровотока - скорость кровотока в конце диастолы)/пиковая систолическая скорость кровотока.
Все данные за исключением наличия или отсутствия ESP выражались как среднее ± стандартное отклонение. Непарный t-тест использовался для сравнения значений в каждой группе. Отсутствие или наличие ESP анализировались с помощью теста хи-квадрат. Регрессионный анализ использовался для оценки отношения между индексами Допплера и диастолическим АД. Значение р менее 0,05 являлось статистически достоверным.
Результаты
Характеристики здоровых пациенток представлены в таблице 1. Срок гестации на время осмотра, возраст беременной и процент первородящих значительно не отличались между группами. Системное артериальное давление значительно различалось между группами (р ≤ 0,001).
Таблица 1.
Характеристика здоровых беременных и пациенток с PIH
| Характеристика | Здоровые пациентки (n=42) | Пациентки с PIH (n=21) | p |
| Возраст, годы | 30,8 ± 3,5 | 31,7 ± 3,4 |
0,57 |
| Первые роды, % | 28 (67) | 15 (71) | 0,92 |
| Срок гестации, недели | 33,5 ± 4,1 | 35,2 ± 3,3 | 0,09 |
| АД, мм рт. ст. | |||
| Систолическое | 113,2 ± 20,5 | 154,2 ± 19,1 | ≤ 0,001 |
| Диастолическое | 69,9 ± 7,9 | 98,7 ± 10,8 | ≤ 0,001 |
Типичные Допплеровские волны у здоровых пациенток и у беременных с PIH представлены на рисунке 1. В обеих группах значительной разницы в индексах между почками отмечено не было.
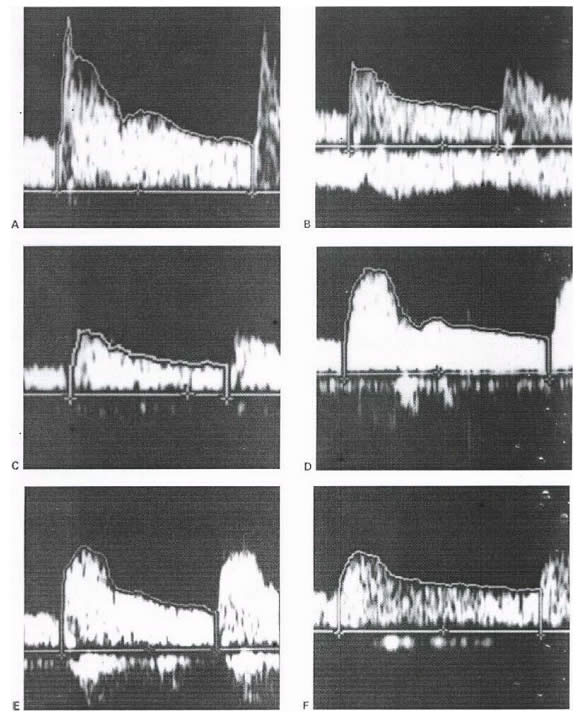 |
| Рисунок 1. Спектральный анализ показывает волны в почечной артерии (А), сегментарных артериях (В), внутридолевых артериях (С) у здоровых беременных по сравнению с почечными артериями (D), сегментарными артериями (Е) и междолевых артериях (F) у пациенток с PIH. У здоровых беременных наблюдается ранняя систолическая эластичность ESP, и угол ранней систолической фазы является острым во всех 3 сосудах. У пациенток с PIH комплекс отсутствует, угол более круглый, а время ускорения более продолжительное в сегментарных и междолевых артериях. |
Пиковая систолическая и конечно-диастолическая скорость кровотока, RI, время ускорения, систолическое ускорение и наличие или отсутствие ESP в главной почечной артерии, сегментарных и междолевых артериях представлены в таблице 2.
Таблица 2.
Анализ волн Допплера главной почечной артерии, сегментарных артерий
и междолевых артерий у здоровых беременных и беременных с PIH
| Почечная артерия | |||
| Характеристика пациента | Здоровые беременные (n = 42) |
Беременные с PIH (n = 21) |
p |
| Пиковая систолическая скорость, м/секунда | 0,67 ± 0,14 | 0,57 ± 0,1 | 0,01 |
| Скорость кровотока в конце диастолы, м/сек | 0,2 ± 0,05 | 0,17 ± 0,04 | 0,08 |
| Индекс сопротивления | 0,7 ± 0,06 | 0,67 ± 0,11 | 0,21 |
| Время ускорения, мсек | 46 ± 12,2 | 77,2 ± 63,4 | 0,02 |
| Систолическое ускорение, мсек | 15,46 ± 5,21 | 11,92 ± 7,3 | 0,06 |
| Ранний систолический пик Есть, кол-во пациентов Нет, кол-во пациентов |
42 0 |
18 3 |
0,06 |
| Сегментарная артерия | |||
| Характеристика пациента | Здоровые беременные (n = 42) |
Беременные с PIH (n = 21) |
p |
| Пиковая систолическая скорость, м/секунда | 0,38 ± 0,08 | 0,38 ± 0,1 | 0,87 |
| Скорость кровотока в конце диастолы, м/сек | 0,13 ± 0,03 | 0,14 ± 0,03 | 0,27 |
| Индекс сопротивления | 0,65 ± 0,06 | 0,64 ± 0,06 | 0,24 |
| Время ускорения, мсек | 59,5 ± 23,6 | 128,2 ± 47.8 | ≤ 0,001 |
| Систолическое ускорение, мсек | 7,1 ± 2,51 | 3,58 ± 2,17 | < 0,001 |
| Ранний систолический пик Есть, кол-во пациентов Нет, кол-во пациентов |
Нет | Нет | Нет |
| Междолевая артерия | |||
| Характеристика пациента | Здоровые беременные (n = 42) |
Беременные с PIH (n = 21) |
p |
| Пиковая систолическая скорость, м/секунда | 0,23 ± 0,05 | 0,24 ± 0,05 | 0,66 |
| Скорость кровотока в конце диастолы, м/сек | 0,08 ± 0,03 | 0,09 ± 0,02 | 0,10 |
| Индекс сопротивления | 0,65 ± 0,07 | 0,62 ± 0,06 | 0,05 |
| Время ускорения, мсек | 55,5 ± 24,2 | 135,4 ± 43,5 | < 0,001 |
| Систолическое ускорение, мсек | 5,02 ± 2,55 | 1,89 ± 0,86 | < 0,001 |
| Ранний систолический пик Есть, кол-во пациентов Нет, кол-во пациентов |
Нет | Нет | Нет |
У трех из 21 пациентки с PIH наблюдалось снижение нормального комплекса ESP в почечной артерии по сравнению с группой здоровых беременных. Однако эта разница не была статистически значима (р = 0,06). У пациенток с PIH пиковая систолическая скорость в почечной артерии была значительно снижена (р = 0,01), а время ускорения более продолжительное (р = 0,02) по сравнению со здоровыми беременными. Однако эти изменения возникают вследствие отсутствия ESP у трех пациенток с PIH.
В сегментарных и междолевых артериях у пациенток с PIH наблюдалось значительное удлинение времени ускорения (р ≤ 0,001) и снижение значений систолического ускорения (р ≤ 0,001) по сравнению со здоровыми беременными. Другие показатели в сегментарных и междолевых артериях значительно не отличались между группами (таблица 2).
На рисунке 2 представлена связь между временем ускорения в междолевой артерии и диастолическим артериальным давлением. Время ускорения значительно повышается с повышением показателя диастолического АД.
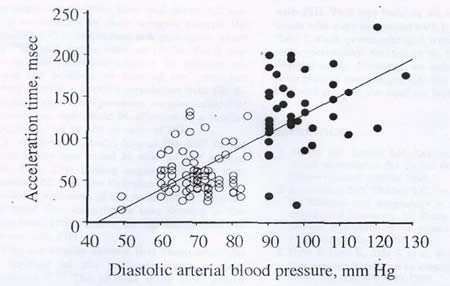 |
| Рисунок 2. График указывает на связь между временем ускорения в междолевой артерии и диастолическим АД. Белые кружки – здоровые беременные, черные кружки – беременные с PIH. Это образует линейную регрессию: АТ = 2,2DBP-95; r2 = 0,52. АТ – время ускорения (мсек), DBP – диастолическое АД (мм рт. ст.). |
Обсуждение
При нормальном течение беременности большое повышение тока плазмы через почку и клубочковой фильтрации возникает вследствие расширения почечных сосудов во втором триместре. За этим следует небольшое снижение в третьем триместре. Увеличение объема плазмы возникает после расширения артериол, что приводит к снижению АД (14). Эти почечные и сердечно-сосудистые механизмы очень важны для успешного течения беременности. Напротив, PIH связана с повышением периферического сосудистого сопротивления в кровотоке матери (15). Повышение сопротивления в почках приводит к снижению тока плазмы через почку и скорости клубочковой фильтрации (2). Таким образом, у пациенток с PIH можно ожидать значительные изменения в почечном кровотоке по сравнению со здоровыми беременными.
Некоторые исследователи пробовали оценить почечный кровоток с помощью Допплера у здоровых беременных (3-5) и у пациенток с преэклампсией или PIH (6-9, 16, 17). Хотя в ходе данных исследований проводилась оценка тех сосудов почек, которые можно увидеть с помощью Допплеровской сонографии, результаты были противоречивыми. Диагностические направления, разработанные в одних лабораториях, не имели подтверждения в других. Однако, параметры, которые анализировали в ходе данных исследований (3-9) были ограничены наиболее общими параметрами дистального сосудистого сопротивления, таких как систоло-диастолическое отношение, RI. В ходе нашего исследования, волновые индексы для сосудистого сопротивления нисходящего потока у пациенток с PIH не отличались от таковых при нормальном течении беременности, даже в междолевых артериях.
В настоящем исследовании авторы исследовали показатели времени ускорения, систолического ускорения и ESP, которые являются гемодинамическими параметрами для значимого восходящего стеноза. Тяжелый стеноз артерии приводит к снижению давления в зоне сразу после стеноза, что приводит к ослаблению пульса в нисходящей артериальной сети, что клинически описывается как pulsus tardus (пульсовая волна медленно поднимается) и pulsus parvus (небольшая амплитуда пульса) (18). В области после стеноза данный феномен наблюдается при Допплеровской сонографии в виде продленного времени ускорения и исчезновения ESP (10). Данный принцип легко применим при оценке почечного кровотока. После работы Handa и коллег (11) началась оценка волны tardus-parvus для диагностики артериального стеноза почечных артерий. Эти исследователи обнаружили снижение систолического ускорения дистальнее места стеноза. Результаты нашего исследования, которые показали наличие продленного времени ускорения и уменьшение систолического ускорения в сегментарных и междолевых артериях у пациенток с PIH, совпадают с результатами наблюдениями за стенозом почечных артерий у небеременных женщин (11, 12). Продленное время ускорения и снижение систолического ускорения в этих артериях указывает на возможность, что спазм сосудов является патогенетическим моментом для развития PIH и приводит к изменениям в дистальных сегментарных и междолевых артериях. Вследствие того, что время ускорения в междолевой артерии указывает на положительную связь с диастолическим АД, авторы предположили, что определение времени ускорения может быть эффективным рутинным методом для диагностики тяжести PIH.
В настоящем исследовании исчезновение ESP в почечной артерии было отмечено лишь у 14% пациенток с PIH. Это указывает на то, что у большинства женщин с PIH сосудистые нарушения не возникают в восходящих отделах почечной артерии. Нарушения кровотока могут возникнуть в главной почечной артерии и/или в сегментарных артериях у пациенток с PIH.
Предыдущие исследования показали, что сужение сосудов вовлечены в патофизиологию преэклампсии (19-23). Настоящее исследование подтверждает эти данные. Сужение сосудов приводит к повреждению эндотелия сосудов, что приводит к вовлечению в процесс различных органов и систем (почки, печень, мозг, система коагуляции) (19). Результаты исследования (20, 23) на крысах и приматах показали, что ингибирование синтеза окиси азота во время нормальной беременности приводит к клинической картине схожей с преэклампсией. Более того, описание положительного влияния окиси азота при лечении HELLP-синдрома, указывает на то, что окись азота вносит свой вклад в развитие гипертензии во время беременности в качестве эндотелиального расслабляющего фактора.
Недавно Kanayama и коллеги (22) показали, что животную модель HELLP-синдрома можно разработать, стимулируя чревный ганглий у крыс. Авторы пришли к выводу, что повторяющийся транзиторный спазм сосудов почечной артерии, вызываемый катехоламинами, приводит к повреждению эндотелия, что ведет к продолжительному спазму сосудов и гипертензии. На основании этих данных мы сделали вывод, что нарушения кровотока при PIH возникает вследствие тяжелого стеноза или продолжительного спазма сосудов. Данный процесс может происходить в основной почечной артерии, сегментарной артерии, а также в более дистальных сосудах.
Авторы отмечают, что исследование было слишком ограничено для определения патогенеза PIH вследствие относительно небольшого количества пациенток с PIH. Вот почему были отобраны пациентки только с диагностированной гипертензией менее недели назад до начала исследования, и которые не успели начать лечение. Однако авторы полагают, что результаты укажут на новый аспект патогенеза PIH и покажут необходимость в новых исследованиях.
Список литературы
- Atrash HK, Koonin LM, Lawson HW, et al. Maternal mortality in the United States. 1979-1986. Obstet Gynecol 1990;76:1055.
- Lindheimer MD, Chelsey LC. Taylor JR, et al. Renal function and morphology in the hypertensive disorders uf pregnancy. In: Sharp F. Symunds EM, editors. Hypertension in pregnancy. New York: Perinatology Press; 1987. p 73.
- Hata T. Hata K, Aoki S, et al. Renal arterial blood flow velocity waveforms in pregnant women. Am J Obstet Gynecol 1987;157:1269.
- Kurjak A, Vidovic MI, Velemir D, et al. Renal arterial resistance index in pregnant and nonpregnant women: evaluation with color and pulse Doppler ultrasound. J Perinat Med 1992,20:11.
- Sturgiss SN, Martin K, Whittingham A. et al. Assessment of the renal circulation during pregnancy with color Doppler ultrasonography. Am J Obstet Gynecol 1992;167:1250.
- Sohn C, Fendel H. The renal aitery and uterine circulation in normal and toxemic pregnancies [in German], Z Geburtshiife Perinatol 1988,192:43.
- Levine AB, Lockwood CJ, Chitkara U, et al. Maternal renal artery Doppler velocimetry in normotensive pregnancies and pregnancies complicated by hypertensive disorders. Obstet Gynecol 1992; 79:264.
- Liberati M, Rotmensch S, Zannolli P, et al. Doppler velocimetry of maternal renal interlobar arteries in pregnancy-induced hypertension. Lit J Gynaecol Obstet 1994;44:129.
- Boemi G, Bruno MT, La Ferrera GL, et al. Maternal renal and interlobar arteries waveforms evaluation with color Doppler ultrasound in pregnancy-induced hypertension. Fetal Diagn Ther 1996;11: 132.
- Kotval PS. Doppler waveform parvus and tardus. A sign of proximal flow obstruction. J Ultrasound Med 1989:8:435.
- Handa N, Fukunaga R, Etani H, et al. Efficacy of echo-Doppler examination for the evaluation of renovascular disease. Ultrasound Med Biol 1988; 14:1.
- Lafortune M, Patriquin H, Demeule E, et al. Renal arterial stenosis: slowed systole in the downstream circulation—experimental study in dogs. Radiology 1992; 184:475.
- Nakai A. Asakura H, Oya A, et al. Pulsed Doppler US findings of renal interlobar arteries in pregnancy-induced hypertension. Radiology 1999:213:
- Baylis C, Deng A, Couser WG. Glomerular hemodynamic effects of late pregnancy in rats with experimental membranous glomerulonephropathy. J Am Soc Nephrol 1.995:6:1197.
- Chesley LC. Hypertensive disorders in pregnancy. New York: Appleton Century Crofts: 1978. Pp 170-175.
- Gudmundsson S. Marsal K. Doppler ultrasound examination of the renal artery in healthy women, normotensive pregnant women and women in preeclampsia. Ultrasound Obstet Gynecol 1991;!;-258.
- Guzman ER, Kappy K, Schulman H. Maternal renal artery flow velocity waveforms in normotensive and hypertensive pregnant women. Journal of Maternal-Fetal Investigation 1991;!: 213.
- Braunwald E. Heart disease. Philadelphia: Saunders; 1981. p 64.
- Roberts JM, Taylor RN, Friedman SA, et al. New developments in pre-eclampsia. Fetal and Maternal Medicine Review 1990:2:125.
- Baylis C, Engles K. Adverse interaction between pregnancy and a new model of systemic hypertension produced by chronic blockade of endothelial desived relaxing factor (EDRF) in the rat. Clinical and Experimental Hypertension. Part B. Hypertension in Pregnancy 1992:11:117.
- Oosterhof H, Voorhoeve PG, Aarnoudse JG. Enhancement of hepatic artery resistance to blood flow in pre-eclampsia in presence or absence of HELLP syndrome (hemolysis, elevated liver enzymes, and low platelets). Am J Obstet Gynecol 1994:171:526.
- Kanayama N, She L, Maehara K, et al. Induction of HELLP syndrome-like biochemical parameters by stimulation of the celiac ganglion in rats. J Hypertens 1996:14:453.
- Podjarny E, Ben-Chetrit S, Rathaus M, et al. Pregnancy-induced hypertension in rats with
Adnamycin nephropathy is associated with an inadequate production of nitric oxide. Hypertension 1997:29:986. - de Belder AJ, Less C, Martin J, et al. Treatment of HELLP syndrome with nitric oxide donor. Lancet 1995;345:124.

