"Тольяттинский медицинский консилиум" 2014г. № 3-4
Лечебно-диагностическая помощь и тактика
консервативного лечения новорожденных детей
c язвенно-некротический энтероколитом
Н.А. Ренц, Н.Н. Хуторская, Е.В. Алексеевнин, С.В. Юрченко, В.Я. Вартанов, С.А. Павловская
МБУЗ СО «Тольяттинская городская клиническая больница № 5» (главный врач – к.м.н. Н.А. Ренц), РФ
Medical-diagnostic aid and tactics of conservative
treatment of newborn children with
ulcer-necrotizing enterocolitis
N.A. Renz, N.N. Hutorskaya, E.V. Alekseevnin,
S.V. Yurchenko, V.Ia. Vartanov, S.A. Pavlovskaya
Резюме
Работа посвящена проблеме лечения некротического энтероколита у новорожденных. Предложена
методика, основанная на многолетнем опыте работы. Подробно описаны клиника, дифференциальная
диагностика, осложнения и лечение, приведены меры профилактики и возможные проблемы
деонтологического характера.Статья может быть интересна неонатологам, реаниматологам.
Ключевые слова: некротический энтероколит, новорожденный, недоношенность
Актуальность.
Достижения неонатологии, связанные с улучшением качества оказания помощи новорожденным с
низкой массой тела, недоношенным, перенесшим хроническую внутриутробную гипоксию и другими неблагоприятными факторами, повысили не только выживаемость таких детей, но и увеличили популяцию
новорожденных с риском развития тяжелых заболеваний желудочно-кишечного тракта [1, 3]. Наиболее
тяжелыми и угрожающими жизни заболеваниями у новорожденных являются язвенно-некротический
энтероколит (ЯНЭК) и перфорации желудочно-кишечного тракта, летальность при которых составляет
40-80%, достигая 100% у пациентов с наиболее тяжелыми формами заболевания и сопутствующими патологическими состояниями [2].
Клиническое течение ЯНЭК и перфораций ЖКТ у новорожденных очень тяжелое, сопровождается
перитонитом, высоким внутрибрюшным давлением с развитием синдрома полиорганной недостаточности. Указанный комплекс патофизиологических процессов определяет развитие жизнеугрожающего состояния для пациента и создает трудности в лечении
Этиология ЯНЭК. Ишемия, перенесенная в перинатальном периоде, аномальная колонизация кишечника новорожденного, неадекватный характер питания ребенка в раннем постнатальном периоде и
инфекционный агент играют важную роль в этиологии заболевания [2, 5].
Факторы риска. Патологическое течение беременности, применении женщиной во время беременности наркотических препаратов, таких, как кокаин, асфиксия в родах, синдром дыхательных расстройств,
значительное охлаждение ребенка (до to ниже 35oС), синдром малого сердечного выброса, при врожденных пороках развития сердца (ВПС), в основном, «синего типа», полицитемия, медикаменты, нарушающие мезентериальный кровоток (индометацин, витамин Е) – наиболее распространенные факторы риска
развития обсуждаемой патологии [3, 14, 18].
Причины развития ЯНЭК. В раннем постнатальном периоде (на 2-4-е сутки жизни) травмирование
сосудов пупочного канатика при кордоцентезе, микротромбозы и тромбоэмболия мезентериальных сосудов. Пободный же механизм развития ЯНЭК предполагается и у детей после катетеризации пупочной
артерии и вены в постнатальной периоде для проведения перфузий, заменного переливания крови, при
различных пороках развития ЖКТ (гастрошизис, болезнь Гиршпрунга, атрезиях кишечника, особенно в
сочетании с синдромом «яблочной кожуры») [10, 11, 18].
По течению заболевания выделяют следующие формы:
- Молниеносная форма. От первых нечетких симптомов дискомфорта в состоянии ребенка до возникновения перфорации проходит не более 1,5-2 суток [5, 13].
- Острая форма. Заболевание начинается с ярко выраженных симптомов со стороны брюшной полости, отказа от еды, срыгиваний и рвот, вздутия живота, нарушение пассажа по кишечнику, что соответствует стадии 1. Вскоре присоединяются общесоматические симптомы, свидетельствующие об интоксикации и дисфункции жизненно важных органов и систем. При неадекватности или неэффективности
консервативной терапии заболевание может быстро перейти в III-ю стадию развития процесса, что требует незамедлительного хирургического лечения.
- Подострая форма. Симптомы со стороны ЖКТ появляются постепенно и имеют перемежающийся характер, т. е. периоды клинического благополучия сменяются возвратом дисфункции со стороны органов ЖКТ. Заболевание развивается медленно, его течение нередко носит рецидивирующий характер[8,11,18].
В зависимости от распространенности процесса выделяют следующие формы:
- Локальная форма - поражение ограничено небольшим участком кишки.
- Мультисегментарная форма – поражено несколько участков кишки.
- Тотальное поражение кишечника или пан-некроз [9,10].
Молниеносная форма ЯНЭК наиболее характерна для доношенных «крупных» детей, перенесших в
родах асфиксию, а также для новорожденных с гемолитической болезнью (особенно после повторных заменных переливаний крови), и для пациентов с пороками развития ЖКТ. Первые симптомы заболевания
при молниеносной форме ЯНЭК появляются несколько раньше (на 3-5 день жизни), чем при других вариантах течения болезни. Своевременная диагностика этой формы заболевания нередко бывает затруднена
из-за преморбидного фона и очень тяжелого общего состояния ребенка. Тем не менее, появление вздутия
живота, беспокойство ребенка, резкое ухудшение лабораторных данных, свидетельствующих о воспалительном процессе, должны навести на мысль о возможном развитии ЯНЭК. Такие дети требуют срочного
осмотра хирурга и рентгенологического обследования.
Острая форма ЯНЭК характерна для недоношенных детей с массой более 1000 г. При этой форме
чаще встречается локальное поражение тонкой кишки, причем от первых симптомов до возникновения
перфорации кишки обычно проходит 2-3 суток. Заболевание начинается остро на 10-28-й день жизни, с
появления признаков поражения ЖКТ. Быстро присоединяются или нарастают общесоматические симптомы, состояние прогрессивно ухудшается. У больных чаще всего выявляют локальное поражение тонкой кишки или некроз стенки желудка, реже мультисегментарное распространение процесса или тотальный некроз кишки.
Подострая форма характерна для глубоко недоношенных детей и детей с критически низкой массой
тела. Первые симптомы появляются на 12- 45-е сутки жизни. Ребенок перестает усваивать питание, начинает срыгивать, возникает вздутие живота, меняется характер стула – он может участиться, в нем появляется примесь зелени и крови, а иногда, наоборот, становится более редким и прекращается вообще.
При подострой форме НЭК нередко в последующем развивается частичная, а затем и полная кишечная
непроходимость, причинами которой могут быть межкишечные абсцессы, инфильтраты или обтурация
кишечника плотными кишечными массами (обтурационная кишечная непроходимость).
Диагностика. Важнейшую роль играет рентгенологическое обследование. Расширение кишечных
петель – наиболее частый симптом. Значительное расширение кишечных петель и появление горизонтальных уровней свидетельствует о тяжести заболевания и его прогрессирующем течении. Пневматоз кишечной стенки (интрамуральное скопление газа) является одним из наиболее важных радиологических
признаков НЭК. Этот симптом чаще определяется в более поздних стадиях заболевания [11, 14]. Поскольку появление газа в стенке кишки связано с жизнедеятельностью микробов, находящихся в кишечнике,
то пневматоз возникает чаще у детей, уже получавших энтеральное питание (84%), чем у пациентов, которые не кормились (16%). На рентгенограмме одного из наших пациентов (см. рис. 1) могут одновременно
определяться два вида пневматоза – кистовидный и линейный.
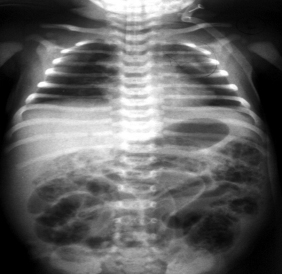
Рис.1. Обзорная рентгенограмма новорожденного С
По мнению некоторых исследователей, пневматоз свидетельствует о необратимой фазе поражения
кишечника, требующей экстренной хирургической помощи [14]. Другие авторы полагают, что пневматоз
не всегда предрекает перфорацию кишки, а поэтому при относительно стабильном состоянии больного
возможно проведение консервативной терапии [18].
Газ в воротной вене (см. рис. 2) – очень грозный признак, часто свидетельствующий о далеко зашедшем процессе. Предполагается, что газ в виде эмболов попадает в систему воротной вены из некротизированной кишечной стенки (с пневматозом) или образуется непосредственно в сосудистых капиллярах
в результате проникновения в эти капилляры газ-продуцирующих бактерий (анаэробов). Наличие газа
в системе воротной вены встречается у 61% детей с тотальным некрозом кишки и предопределяет неблагоприятный прогноз, поэтому наличие данного симптома является абсолютным показанием к хирургическому лечению. Наличие неподвижной (статичной) петли кишки, не изменяющей свое положение
на повторных снимках, свидетельствует о кишечной ишемии. Такие петли могут быть локализованными,
единичными, или множественными. Сопоставление рентгенограмм, сделанных с некоторым интервалом
во времени (6 – 8 часов), помогают отдифференцировать обычное расширение кишечных петель от фиксированных и неподвижных участков. Многие исследователи считают этот симптом патогномоничным
для некроза кишки, и, соответственно, позволяющим ставить показания к операции.
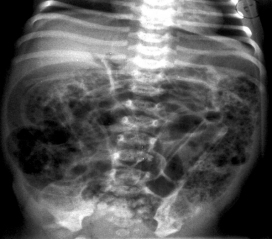
Рис. 2. Обзорная рентгенограмма новорожденного Р
Снижение пневматизации и неравномерное газонаполнение кишечных петель объясняется тем, что
в результате активной перистальтики кишечное содержимое продвигается из жизнеспособных отделов
кишки в ишемически пораженные, в которых перистальтика либо снижена, либо полностью отсутствует.
Эти отделы кишечника, как правило, бывают заполнены жидким содержимым, что также способствует
снижению количества находящегося в них газа. Его выявление позволяет продолжить консервативную
терапию с тщательным контролем за состоянием ребенка и изменением рентгенологической картины.
Внезапное появление на рентгенограммах признаков асцита, выявляемых у 11% больных, является
неблагоприятным фактором, говорящим о реакции брюшины на бактериальный перитонит, о возможной
прикрытой перфорации кишки. Сочетание асцита и появления газа в воротной вене сопровождается с
высокой смертностью пациентов [19].
Расширение желудка – еще один симптом ЯНЭК, выявляемый на обзорных рентгенограммах и обусловленный как атонией желудка, вызываемой воздействием бактериальных токсинов, так и псевдообструкцией пилорического отдела в результате отека слизистой.
Пневмоперитонеум – скопление свободного газа в брюшной полости, чаще под куполами диафрагмы
у детей с ЯНЭК неопровержимо свидетельствует о перфорации полого органа (см. рис. 3). Этот симптом
был выявлен лишь у 63% наших пациентов, у которых на операции была обнаружена перфорация. Отсутствие на рентгенограмме газа в свободной брюшной полости при наличии перфорации объясняется тем,
что перфорация может быть прикрытой или «открываться» в карман или полость сальниковой сумки,
изолированных от свободной брюшной полости.
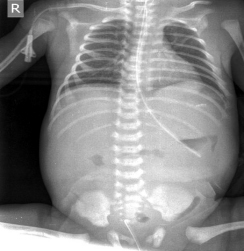
Рис. 3. Обзорная рентгенограмма новорожденного К.ЯНЭК III – IV, газ в свободной брюшной полости
УЗИ органов брюшной полости и забрюшинного пространства используется для выявления выпота
в брюшной полости, обнаружения инфильтратов и абсцессов. На рис. 5 представлена УЗИ- картина пневмоперитонеума.
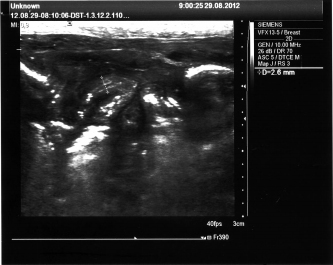
Рис. 4. УЗИ органов брюшной полости и забрюшинного пространства.
Воздух в брюшной полости
Лапароцентез (см. рис. 5) – достаточно часто использующийся в нашей практике метод экспресс-диагностики.
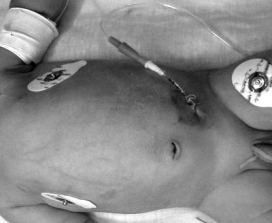
Рис. 5. Лапароцентез
Получение из брюшной полости при аспирация более, чем 1,0 мл желто-коричневого или зеленого, мутного содержимого свидетельствует о некрозе кишки.
Абсолютные показания к хирургическому лечению:
- Появление в брюшной полости пальпируемого опухолевидного образования, свидетельствующего о наличии внутрибрюшного абсцесса или конгломерата спаянных между собой некротизированных
кишечных петель.
- Воспалительные изменения брюшной стенки, которые обычно появляются при наличии перитонита, гангрены кишки или подлежащего к брюшной стенке абсцесса.
- Специфическая рентгенологическая картина, свидетельствующая о гангрене кишки - наличие статичной, «стабильной» петли кишки, неравномерное вздутие кишечных петель, пневматоз кишечной стенки, газ в воротной вене, признаки асцита.
- Лабораторные данные - остро развившаяся тромбоцитопения, коагуляционные нарушения, тяжелая гипонатриемия и стойкий ацидоз.
- Лабораторные данные - остро развившаяся тромбоцитопения, коагуляционные нарушения, тяжелая гипонатриемия и стойкий ацидоз.
- Лабораторные данные - остро развившаяся тромбоцитопения, коагуляционные нарушения, тяжелая гипонатриемия и стойкий ацидоз.
- Данные абдоминального парацентеза: получение мутной, коричневой или зеленоватой жидкости,
выявление в содержимом большого количества лейкоцитов, а при окраске по Граму - внеклеточных бактерий [4, 5, 6, 7, 9].
Лечение некротического энтероколита зависит от стадии заболевания и степени выраженности симптомов, складывается из консервативного и хирургического этапов.
Консервативное лечение некротического энтероколита [12, 15, 17, 20]
- Энтеральное питание - режим трофического кормления (1ml| kg - микроструйное введения) при НЭК I ст.
При малейшем подозрении на НЭК IIа ст. - отмена энтерального питания
Постановка в желудок для декомпрессии постоянного назогастрального или орогастральнога зонда (держать открытым)
- Респираторная терапия (ИВЛ, неинвазивная вентиляция легких).
- Антибактериальная терапия.
(Карбапенемы + гликопептиды или комбинированные цефалоспорины)
Схемы антибактериальной терапии представлена в таблице № 1.
Таблица 1.
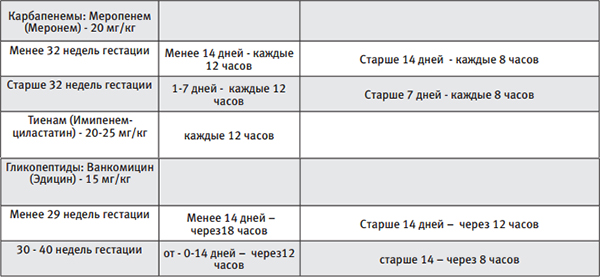
При выделении вероятного возбудителя – смена антибактериальной терапии с учетом спектра его
чувствительности.
- Препарат глутамина для парентерального питания (Дипептивен – 2 мл/кг)
- Седация и аналгезия (наркотические аналгетики (фентанил – 1-3 мкг/кг/ч),
Бензодиазепины ( седуксен 0,02 – 0,3 мг/кг), согласно шкале СRIES.
Натрия оксибутират (100 -200 мг/кг/мин)
- Добутамин – 2 – 15 мкгр/кг/ч – обладает выраженным инотропным эффектом(септический шок)
- Полигаммаглобулины(Пентоглобин – 5 мл/кг)
- Гемо - и плазмотрансфузия(по показаниям)
- Симптоматическая терапия и терапия патологического состояния, которое было первичным у ребенка и потенцировало развитие НЭК.
- Полное парэнтеральное питание (TPN).
Основной принцип TPN – сбалансированность всех компонентов (белков, жиров, углеводов, микро-
элементов, витаминов).
Критерии для проведения TPN:
- TPN необходимо назначать при развитии ЯНЭК II-III стадии и продолжить в ранние сроки после хирургического лечения (3-5сутки).
- Для назначения TPN необходимо добиться полной стабилизации состояния больного (коррекция метаболических нарушений и КОС, стабилизация гемодинамики, отмена планового наркотического обезболивания).
TPN начинают детям рожденным с m<1500 г или новорожденным, которые не могут получить энтеральное питание, обеспечивающее им 80-90 Ккал/кг/сут. к концу 1 недели жизни. Схема TPN представлена в таблице № 2.
Таблица 2.
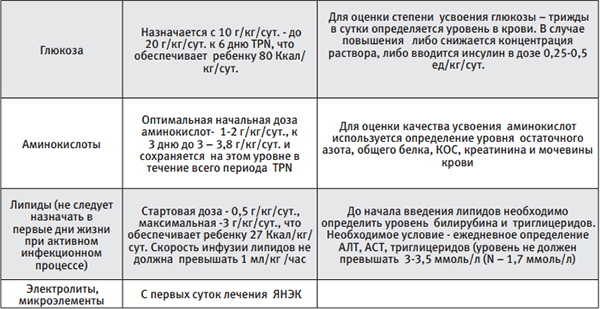
Период энтерального голода в группе детей, получающих консервативное лечение, которое оказывается эффективным, недлительный, редко превышает 7-8 дней. Энтеральное кормление возобновляется с того
момента, как у ребенка восстанавливается пассаж по кишечнику, исчезает вздутие живота, появляется стойкая тенденция к улучшению или нормализации лабораторных показателей и рентгенологических данных.
Наилучшим видом питания для новорожденного ребенка, конечно, является грудное молоко. Однако,
после тяжелых воспалительных заболеваний ЖКТ, длительной антибактериальной терапии развивается
тяжелый дисбактериоз и вторичная лактазная недостаточность, поэтому при введении даже грудного
молока у больного могут усиливаться бродильные процессы, страдать переваривание и всасывание.
В связи с этим, в качестве первой смеси для энтерального питания можно использовать безлактозную или гиполактозную смесь типа Альфаре (компания «Nestle»), Нутрисоя.
По мере повышения толерантности организма к вводимой смеси, стабилизации весовых прибавок
ребенка постепенно переводят на вскармливание грудным молоком.
Профилактика некротического энтероколита
Профилактика ЯНЭК должна начинаться еще до рождения ребенка. Заместительная терапия внутривенным человеческим иммуноглобулином «Пентаглобин» оптимальный выбор антибактериальной терапии с лабораторным контролем ее эффективности соблюдение правил введения энтеральной нагрузки
(2-3 мл у недоношенных и 5-10 мл у доношенных детей на прием) [18, 20, 21, 22].
Деонтологические проблемы
Так как ухудшение состояния детей группы высокого риска развития НЭК часто происходит на фоне
мнимого благополучия без выраженных клинических симптомов, актуальными являются деонтологические проблемы. Высокая вероятность хирургического вмешательства и неопределенный прогноз еще
больше осложняют ситуацию в отношениях между медицинским персоналом и родителями ребенка. В
связи с этим медицинский персонал должен устанавливать доверительные отношения с родственниками
и достоверно информировать их о текущем состоянии больного и прогнозе для него [14, 16].
Настороженность в отношении развития ЯНЭК у детей группы риска, соблюдение правил введения
энтеральной нагрузки, повышение защитной функции кишечника, отработанный алгоритм ведения этих
детей по стадиям процесса до и после оперативного вмешательства, ранняя диагностика осложнений
ЯНЭК, парентеральное питание с постепенным переходом на энтеральное, последующая реабилитация
совместно с реаниматологом, хирургом, неврологом позволяют остановить процесс на более ранних стадиях и снизить летальность среди детей группы риска по развитию ЯНЭК.
Выводы
К группе риска по развитию ЯНЭК относятся недоношенные дети, перенесшие гипоксию в родах, а
также угрожаемые по развитию интранатальной и внутриутробной инфекции.
- Новорожденные должны консультироваться детским хирургом при появлении первых симптомов ЯНЭК, до развития хирургических осложнений.
- Улучшение результатов лечения ЯНЭК возможно лишь при тесном взаимодействии врачей различных специальностей, занимающихся выхаживанием недоношенных детей.
Литература
- Александрович Ю.С. Пшениснов К.В. «Интенсивная терапия новорожденных» 2013г. с 173 - 188 с. 411- 421
- Баиров Г. А. Рошаль Л. М. Острые гнойные заболевания новорожденных // Гнойная хирургия детей: Руководство для врачей.Л. : Медицина, 1991. - С. 254 - 264.
- Володин Н. Н., Коршунов В. М., Агафонова С. А. Защитная система желудочно-кишечного тракта у детей / // Вопросы гинекологии, акушерства и перинатологии. 2004. - Т. 3, № 2. - С. 62 - 67.
- Головко О.К., Левицкая Е.М., Линчевский Г.Л. Особенности ведения новорожденных с некротизирующим энтероколитом // Архив клинической и экспериментальной медицины. — Т. 11, № 2. — 2002. — С. 241-244.
- Караваева С. А. Диагностика и особенности клинического течения некротического энтероколита у детей //Вестник хирургии. — 2002. Т. 161, № 4. - С. 41-44.
- Караваева С. А. Хирургическое лечение некротического энтероколита :автореф. дисс. . д-ра мед. наук /СПб., 2002.
- Козлов В.К. Сепсис Спб. «Диалект». - 2006 г.
- Миронов П.И. Терминология педиатрического сепсиса: прошлое, настоящее, будущее // Интенсивная терапия 2006 г., - №1.- с 49 - 55.
- Неонатология . Национальное руководство. Под редакцией академика РАМН проф. Н.Н. Володина 2008 г. с. 447 - 454
- Ситко Л. А. Критерии тяжести и прогноза некротизирующего энтероколита у новорожденных / // Детская хирургия. 2003. - №6. - С. 46 - 48.
- Цап Н. А. Хирургическое лечение и прогнозирование послеоперационного периода у новорожденных с некротическим энтероколитом // Детская хирургия. 2004. -№ 2. - С.13-15
- Чубарова А. И. Некротизирующий энтероколит у новорожденных: новые аспекты патогенеза / Вопросы гинекологии, акушерства и перинатологии. 2003. - Т. 2, № 1. - с. 62-70.
- Шабалов Н. П. Неонатология : Учебное пособие : в 2 т., Т. 1., 3-е изд. - М.: МЕДпресс-информ, 2004. с.341 - 350
- Фармакологический справочник NEOFAX, 2010 – 2011 год
- Albanese С. T. Necrotizing enterocolitis / С. T. Albenese, M. I. Rowe // Pediatric Surgery. 5th ed. / ed. by J. A. O’Neill et al. - Mosby-Year Book, Inc.,1995.-P. 1297-1320.
- R. Beck et al. Abdominal compartment syndrome in children / // Pediatr. Crit. Care Med. 2001. - Vol. 2, N 1. - P. 51-56.
- H. Okuyama et al. Comparison of the clinical presentation and outcome of focal intestinal perforation and necrotizing enterocolitis in very-low-birth-weight neonates / // Pediatr. Surg. Int. 2002. - Vol. 18, N 8. - P. 704 - 706.
- Nelson Textbook of Pediatrics – 18 -19 th edition.
- Richard A.Polin & John M.Lorenz. Neonatology (Cambridge Pocket Clinicians) 2008 P.230 – 233.
- Patti J. Thureen William W. Hay Neonatal Nutrition and Metabolism - 2nd edition. Cambridge 2012
- Ostlie DJ., Spilde T.L., St Peter S.D. et al. Necrotizing enterocolitis in full-term infants // J. Pediatr/Surg. – 2003. – Vol. 38(7) – P.1039-1042
- Grave GD, Nelson SA, Walker WA, et al. New therapies and preventive approaches for necrotizing enterocolitis: report of a research planning workshop. Pediatr Res. 2007;62:510–4.
|

