двухмесячный научно-образовательный журнал
"Тольяттинский медицинский консилиум" 2016г. № 3-4Оценка системы «мать-плод-новорожденный» с позиции перинатальной хрономедициныИ.С. Липатов1, Ю.В. Тезиков1, С.А. Рябова1, О.А. Кутузова2, Т.А. Тезикова2, Н.Н. Данилова1, Р.Я. Ильяшевская3 1Самарский государственный медицинский университет
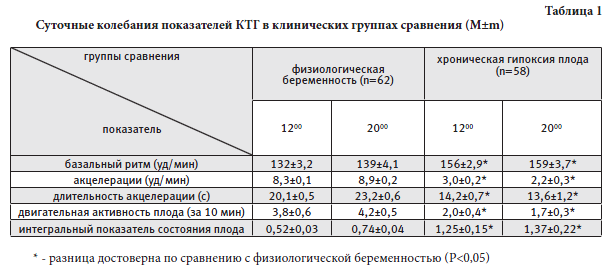
Evaluation of the system «mother-fetus-newborn» from the perspective of perinatal chronomedicineI.S. Lipatov, Yu.V. Tezikov, S .A. Ryabova, O.A. Kutuzova, T.A. Tesikova, N.N. Danilova, R.J. Ilashevskaya РезюмеЦелью исследования явилось совершенствование диагностики и прогнозирования состояния «позднего» плода и новорожденного при плацентарной недостаточности с позиции выявленных особенностей биоритмов основных физиологических функций и уровня адаптивных гормонов. В соответствии с правилами Международного общества хронобиологов обследовано 120 женщин в третьем триместре беременности, их плоды и новорожденные: I группу составили 62 женщины с физиологической беременностью; II группу – 58 женщин с хронической гипоксией плода. Для оценки состояния фетоплацентарного комплекса проводился мониторинг показателей кардиотокографии, ультразвуковой допплерографии, уровней неконъюгированного эстриола и прогестерона сыворотки крови беременных. На 1-4 сутки и 5-7 сутки у новорожденных исследовались биоритмы артериального давления, частоты сердечных сокращений, дыхательных движений, температуры тела, экскреции кортизола, 6-сульфатоксимелатонина, адреналина, норадреналина. Результаты исследования показали, что учет хронобиологических особенностей в оценке состояния фетоплацентарного комплекса, ранней диагностике хронической гипоксии плода, течении раннего неонатального периода у новорожденных расширяет возможности практического акушерства и неонатологии. Раннее прикладывание к груди, совместное пребывание матери и ребенка в послеродовом периоде, свободный режим вскармливания способствуют более раннему становлению биоритмов физиологических показателей жизнедеятельности и благоприятному течению адаптационных процессов у новорожденных. Ключевые слова: биоритмы, фетоплацентарный комплекс, хроническая гипоксия плода, неонатальный период ВведениеОпыт клинической и экспериментальной перинатологии на современном этапе подтверждает ценность динамического подхода в определении функционального состояния систем жизнеобеспечения плода, поскольку любые физиологические показатели имеют временной разброс, обусловленный эволюцией живой матери и астрономическими причинами [1-7]. Однако, до настоящего времени доминирует оценка функциональных показателей, основанная на единичных замерах, которые являются основой для создания нормативных шкал [8-12]. Целью исследования явилось совершенствование диагностики и прогнозирования состояния «позднего» плода и новорожденного при плацентарной недостаточности с позиции выявленных особенностей биоритмов основных физиологических функций и уровня адаптивных гормонов. Пациент и методыДля реализации поставленной цели обследовано 120 женщин в третьем триместре беременности, их плоды и новорожденные в раннем неонатальном периоде на 1-4 и в 5-7 сутки жизни. С учетом течения беременности, состояния плода и новорожденного были выделены две клинические группы сравнения. I группу составили 62 женщины с физиологической беременностью, закончившейся рождением здорового ребенка при гестационном сроке 38-40 недель. Из них 28 женщин родоразрешены путем операции кесарева сечения в связи с тазовым предлежанием и неправильным положением плода, узким тазом, осложненной миопией. У 34 женщин роды протекали через естественные родовые пути (у 30 - самопроизвольные, у 4 - программированные). Часть новорожденных детей для более быстрого восстановления диады «мать-новорожденный» рано прикладывались к груди, были помещены с матерями в палаты совместного пребывания со свободным режимом вскармливания (15 детей, рожденных оперативным путем, и 20 детей, рожденных через естественные родовые пути), остальные находились отдельно от матерей, их кормление осуществлялось «по часам» (13 и 14 детей, рожденных соответственно абдоминальным и естественным методами родоразрешения). II группу составили 58 женщин, у которых беременность в III триместре осложнилась плацентарной недостаточностью с хронической гипоксией плода. Все беременные были родоразрешены в сроке 37-40 недель. Из них 19 женщин родоразрешены путем операции кесарева сечения в интересах плода, у остальных 39 женщин роды происходили через естественные родовые пути (24 - самопроизвольные, 15 - индуцированные). В исследование были включены только женщины, дети которых были рождены в состоянии легкой асфиксии (по шкале Апгар на 1 мин. - 6 баллов; на 5 мин. - 7 баллов; на 30 мин. - 8 баллов) и не требовали реанимационных мероприятий и интенсивной терапии. В палаты совместного пребывания со свободным режимом вскармливания было помещено 34 ребенка (14 детей, рожденных оперативным путем, и 20 детей - через естественные родовые пути), эти дети рано прикладывались к груди; раздельно от матерей пребывало 24 новорожденных, их кормление осуществлялось «по часам» (5 и 19 детей, рожденных соответственно абдоминальным и естественным путями). Организация исследования соответствовала установленным правилам Международного общества хронобиологов [1] . В пределах 36 часов с 4-х часовыми интервалами времени, начиная с 8 часов утра, у женщин и их плодов проводили: мониторинг показателей кардиотокографии (КТГ) и ультразвуковой допплерографии (УЗДГ) с цветным допплеровским картированием кровотока в маточной и пуповинной артериях с определением систоло-диастолического показателя (Vs/Vd) материнского и плодового кровотоков и расчетом коэффициента их синхронизации (Sf); исследование уровня неконъюгированного эстриола (НЭ) и прогестерона (П) в сыворотке крови беременных с подсчетом соотношения НЭ/П. Динамическая оценка клинического состояния новорожденных проводилась на 1–4 и в 5–7 сутки жизни и включала мониторинг основных физиологических показателей (артериального давления (АД), частоты сердечных сокращений (ЧСС), частоты дыхательных движений (ЧДД), аксиллярной и базальной температуры тела (T°акс и T°баз) с помощью витального монитора «SCHILLER»; исследование экскреции адаптивных гормонов с порционной мочой (кортизола (К), 6-сульфатоксимелатонина (6-СТМ), адреналина (А) и норадреналина (НА)) в зависимости от смены цикла «сон-бодрствование»: через 30 минут после засыпания – в период глубокого сна – и в первые минуты после пробуждения, в течение 36 часов, начиная с 8 часов утра. В работе использовались микрометодики радиоиммунологического анализа (стандартные наборы KYT, Германия) для определения уровня НЭ, П, К, 6-СТМ. Концентрация А и НА у новорожденных определялась флюориметрическим методом [23, 24]. Регистрацию КТГ с оценкой интегрального показателя состояния плода – ПСП (ПСП<1,0 соответствует состоянию «здоровый плод»; 1,0≤ПСП<2,0 – «начальные нарушения состояния плода»; 2,0≤ПСП<3,0 – «выраженные нарушения состояния плода»; ПСП≥3,0 – «резко выраженные нарушения состояния плода») производили на полностью автоматизированном компьютерном кардиотокографе АУСП-1 (фирма «Уникос»). В работе использован ультразвуковой аппарат «Philips Tangens». Состояние фетоплацентарного комплекса оценивали по шкале М.И. Кузнецова с соавт. [25, 26], включающей УЗ-фетометрию, определение ЧСС, двигательной активности, тонуса плода, количества околоплодных вод, исследование плаценты. Для определения типов синхронизации в маточно-плацентарно-плодовом комплексе (МППК) рассчитывали Sf, представляющий собой величину, обратно пропорциональную коэффициенту вариабельности модулирующих частот в спектрах, регистрируемых функциональных показателей матери, плода и новорожденного: Sf=1/V, где V – коэффициент вариабельности отношения модулирующих частот Т1/Т2, где Т – длина наибольшего периода в спектре. При оценке межфункциональных связей выделяли 3 типа синхронизации: гиперсинхронный (ГС) - Sf>3,5; синхронный (СХ) - 3,0≤Sf≤3,5; асинхронный (АС) - Sf<3,0. Информативность диагностических исследований оценивалась основными критериями доказательной медицины: чувствительностью, специфичностью, точностью, числом ложноположительных и ложноотрицательных ответов [27, 28]. Периоды ритмов группировались по диапазонам, установленным Международным обществом хронобиологов [29-31]. Обработку временных рядов осуществляли с использованием пакета программ EXCEL 97, входящего в MICROSOFT OFFICE с модулем статистических расчетов, реализованным на языке VISUAL BASIC; Statistica 5,0, из которого использовались программы факторного, кластерного и спектрального анализа. Для выявления характера ритмов применяли теорему Котельникова – Шенона с последующим использованием метода быстрого преобразования Фурье для получения коэффициентов приближенного ряда. При анализе хронограмм показателей оценивались: мезор (Мз) – среднее значение полезного сигнала; амплитуда (Ам) колебаний ритма; акрофаза (Ак) и батифаза (Бт) – время наибольшего и наименьшего значений исследуемого показателя; период ритма – длительность совершения одного цикла колебаний. Для расчета необходимого количества измерений (случаев) применялся метод математического планирования [25]. При этом определялся минимальный объем выборок, который обеспечивал достоверность полученных результатов (95%) и ошибку (±5%), допустимую в медицинских исследованиях. РезультатыАнализ полученных данных суточного ритмостаза уровней фетоплацентарных гормонов, показателей КТГ и гемодинамики материнских и плодовых кровотоков (УЗДГ) как при физиологической беременности, так и при хронической гипоксии плода, показал, что проведение мониторинга гормонального профиля с расчетом показателя НЭ/П наиболее информативно в утреннее (800 час) и вечернее (2000 час) время, а КТГ И УЗДГ в дневное (1200 час) и вечернее (2000 час) время. В эти часы регистрируются максимальные (акрофазы) и минимальные (батифазы) значения диагностически значимых показателей, что дает возможность зафиксировать наибольшие отклонения в состоянии плода. Результаты исследования КТГ при физиологической и осложненной гипоксией плода беременности представлены в таблице 1.
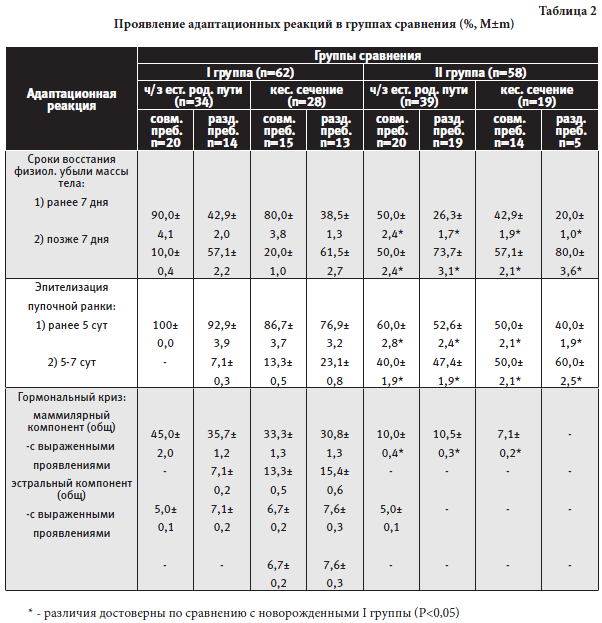
Ритмометрия уровней НЭ и П в сыворотке крови у беременных с физиологическим течением гестации и хронической гипоксией плода показала следующие значения показателя соотношения НЭ/П: в норме показатель в 800 равен 1,52±0,2, в 2000 - 1,5±0,1; при внутриутробном страдании плода в 800 - 0,57±0,05, в 2000 - 0,67±0,06. Межгрупповые различия достоверны как в утренние, так и в вечерние часы (P<0,05). При оценке межфункциональных связей в МППК по показателям гемодинамики (Vs/Vd) материнского и плодового кровотоков были получены следующие данные. Коэффициент синхронизации при физиологической гестации до 37 недель беременности соответствует 3,24±0,16, в этом сроке у всех обследованных беременных отмечен СХ тип связи материнского и плодового кровотоков. После 37 недель Sf соответствует 4,08±0,24, отмечается ГС тип межфункциональных связей. При хронической гипоксии плода в третьем триместре беременности независимо от срока гестации имеет место АС тип связи материнского и плодового кровотоков. Коэффициент синхронизации до 37 недель беременности - 2,35±0,19, после 37 недель беременности - 2,78±0,18. По исходам для плода с позиций доказательной медицины были определены чувствительность, специфичность, точность прогностическая ценность положительного и отрицательного результатов данного метода диагностики хронической гипоксии плода (комплексная оценка состояния МППК с учетом биоритмов показателей КТГ, НЭ/П, Sf), которые соответственно равны 95,3%, 98,8%, 98,3%, 91% и 98%, что свидетельствует о высокой информативности и достоверности разработанного способа диагностики. С точки зрения приспособляемости новорожденных детей к внеутробному существованию в зависимости от течения поздних сроков гестации, метода родоразрешения, вариантов восстановления диады «матьдитя» в послеродовом периоде представляют интерес клиническая выраженность, длительность и сроки появления адаптационных реакций: восстановления физиологической убыли массы тела, эпителизации пупочной ранки, проявлений маммилярного (у мальчиков и девочек) и эстрального (у девочек) компонентов гормонального криза. Течение постнатальной адаптации у обследованных детей представлено в таблице 2.
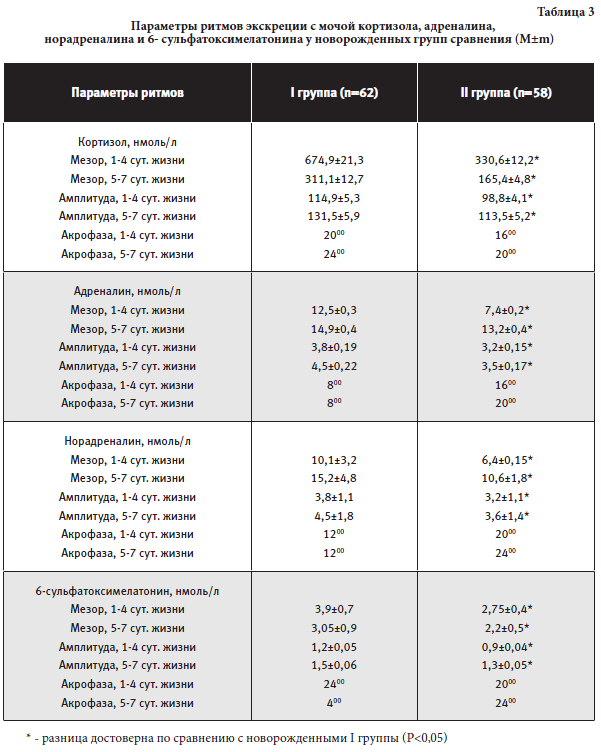
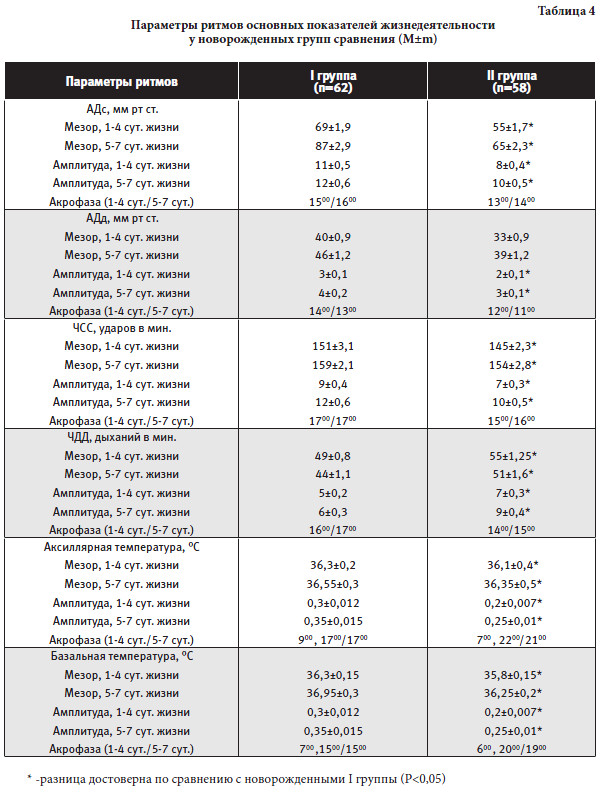
В обеих группах сравнения более раннее восстановление массы тела, заживление пупочной ранки, более частое проявление гормонального криза было у новорожденных от матерей, у которых роды проходили через естественные родовые пути, находящихся в послеродовом периоде в палатах совместного пребывания со свободным режимом вскармливания, с ранним прикладыванием к груди. Результаты ритмометрии уровней экскреции с мочой К, А, НА и 6-СТМ и основных показателей жизнедеятельности у новорожденных групп сравнения представлены в таблицах 3 и 4.
В обеих обследованных группах новорожденных выявляется циркадианная (на 1-4 сут.- 14% у здоровых новорожденных и 4% при хронической гипоксии; на 5-7 сут. - 21% и 10% соответственно) и ультрадианная (на 1-4 сут. - 86% у здоровых новорожденных и 96% при хронической гипоксии; на 5-7 сут. - 79% и 90% соответственно) ритмичность экскреции гормоном с мочой и показателей функций жизнеобеспечения (АД, ЧСС, ЧДД, Тº тела) с преобладанием ультрадианного периода, связанного с ритмами «сон-бодрствование» и «свет-темнота», и постепенным повышением доли циркадианной составляющей по мере увеличения постнатального возраста. При этом у новорожденных с хронической внутриутробной гипоксией ритмичность формируется через 24 часа, а у здоровых новорожденных через 12 часов внеутробной жизни. ОбсуждениеВ последние десятилетия в практическое акушерство широко внедрены нормативные показатели, характеризующие состояния беременных в различные триместры гестации, объединенные понятием «норма беременности» [8]. Однако, хронофизиологической «нормы беременности» до настоящего времени не разработано. Проведенное исследование биоритмов в МППК и у новорожденных позволило установить ряд показателей, которые объективно характеризуют хронофизиологический профиль фетоплацентарной системы в третьем триместре беременности и адаптационные процессы у детей в раннем неонатальном периоде. Ритмометрия функциональных показателей жизнеобеспечения плода (сердечной деятельности, трофоадаптивных гормонов, синхронизации материнского и плодового кровотоков) в отличие от единичных замеров без учета биоритмов в МППК позволяет эффективно контролировать внутриутробное состояние «позднего» плода и своевременно диагностировать хроническую гипоксию. Изменение показателей, предложенных для характеристики состояния фетоплацентарного комплекса, свидетельствует о срыве адаптационных возможностей плода и необходимости их интенсивной коррекции вплоть до досрочного родоразрешения. Положительный эффект разработанного метода диагностики заключается в принципиально новой возможности своевременной диагностики гипоксии плода благодаря новому подходу к оценке используемых параметров. Метод неинвазивен, безопасен для здоровья беременной и плода, доступен для современных учреждений родовспоможения, может широко применяться в массовых профилактических обследованиях как скрининговый с выявлением точных и ранних признаков внутриутробной гипоксии плода. Результаты, полученные в ходе настоящего исследования, подтвердили негативное влияние хронической внутриутробной гипоксии на состояние новорожденного. У детей, рожденных в состоянии асфиксии вследствие прогрессирующей в родах хронической гипоксии, дезадаптация в раннем неонатальном периоде выражалась, согласно полученным данным, в позднем восстановлении первоначальной массы тела, в увеличении сроков эпителизации пупочной ранки, в снижении частоты проявлений гормонального криза. Это свидетельствует об отклонениях от физиологической нормы обмена веществ, трофики тканей, о недостаточной зрелости и реактивности эндокринной, нервной и иммунной систем у данного контингента новорожденных. Изучение экскреции гормонов с порционной мочой у новорожденных обеих групп сравнения (К, А, НА, 6- СТМ) и уровней функциональных показателей (АД, ЧСС, ЧДД, T°акс. и T°баз.) выявило отчетливую ультрадианную хроноструктуру их ритмов, синхронизированную с циклом «сон-бодрствование» (Бт – в период глубокого сна, Ак – через несколько минут после пробуждения) с постепенным возрастанием циркадианной составляющей по мере увеличения постнатального возраста. У здоровых детей появление циркадианной ритмичности изменений экскреции гормонов, температуры и дыхания происходило через 12 час после рождения, гемодинамических показателей – через 18 час и лишь через 24 и 30 час – у новорожденных, перенесших асфиксию. Совокупный анализ всех изученных параметров позволил выявить более раннее становление биоритмов функциональных показателей и экскреции трофоадаптивных гормонов с мочой, благоприятное течение ранней постнатальной адаптации у здоровых новорожденных, рожденных через естественные родовые пути с последующим ранним восстановлением диады «мать-ребенок» (раннее прикладывание к груди, совместное пребывание матери и ребенка в послеродовом периоде, свободный режим вскармливания). У новорожденных с хронической внутриутробной гипоксией при тех же условиях наблюдалось менее благоприятное течение ранней постнатальной адаптации, с ухудшением адаптационных реакций у новорожденных при индуцированных и программированных родах, плановом и срочном кесаревом сечении и поздним восстановлением диады «мать-ребенок» (позднее прикладывание к груди, раздельное пребывание матери и ребенка в послеродовом периоде, режим вскармливания «по часам»). ЗаключениеУчет хронобиологических особенностей в оценке состояния фетоплацентарного комплекса, ранней диагностике хронической гипоксиии плода, течении раннего неонатального периода у новорожденных расширяет возможности практического акушерства и неонатологии и несомненно позволит снизить частоту осложнений во время беременности, родов, послеродовом и постнатальном периодах. Раннее прикладывание к груди, совместное пребывание матери и ребенка в послеродовом периоде, свободный режим вскармливания способствуют более раннему становлению биоритмов физиологических показателей жизнедеятельности и благоприятному течению адаптационных процессов у новорожденных. Литература
|