Сравнительное исследование исходов для матери и плода при использовании эпидуральной анестезии либо раствором бупивакаина, либо ропивакаина в сочетании с фентанилом для обезболивания родов
D. Bolukbasi, E.B. Sener,
B. Sarihshan, S. Kokamanoglu, A.Tur
Цель исследования : Определение максимально безопасного как для матери, так и для плода метода обезболивания родов. Нашей целью было сравнение эффективности и побочных эффектов эпидуральной анестезии растворами бупивакаина или ропивакаина в низких концентрациях в сочетании с фентанилом.
Материалы и методы: В исследование были включены 40 рожениц с оценкой степени риска по шкале ASA I - II . Исследование было проспективным, двойным слепым и рандомизированным, пациентки получали эпидуральную анестезию либо бупивакаином, либо ропивакаином. Вначале вводили 8 мл 0.125% раствора препарата с добавлением 50 мкг фентанила, затем обезболивание поддерживалось постоянной инфузией 0.0625% раствора препарата с добавлением фентанила в концентрации 2 мкг/мл.
Результаты: Никакой значительной разницы оценки по визуальным аналоговым шкалам боли, общим дозам использованного местного анестетика, степени моторного и сенсорного блока, общей продолжительности родов, методам родоразрешения, побочным эффектам, оценкой качества обезболивания пациенткой или исходами для новорожденных между двумя группами зафиксировано не было. Ни в том, ни в другом случае не удавалось достигнуть адекватного обезболивания второго периода родов.
Выводы: Мы не обнаружили никаких существенных различий между эпидуральной анестезией в родах с применением бупивакаина или лидокаина. Мы считаем, что для обеспечения обезболивания второго периода требуется индивидуальный подход к каждой женщине, возможно, с применением разных доз местных анестетиков и методов обезболивания.
Ключевые слова: эпидуральная анестезия в родах, ропивакаин, бупивакаин, эффективность, исход для матери и плода.
Введение
Родовая боль, как и другие виды острой боли, оказывает отрицательное влияние практически на все системы организма: легкие, сердце, сосуды, нейроэндокринные органы и лимбическую систему. Ранее уже были проведены многочисленные исследования, в которых предпринимались попытки найти безопасный метод обезболивания родов, который бы не оказывал побочного действия ни на мать, ни на плод (1-4). Эпидуральная анестезия – это эффективный метод обезболивания родов, однако она может вызывать моторный блок, а это повышает число осложнений в родах и снижает оценку качества метода пациентками.
Для проведения эпидуральной анестезии в родах широко применяются такие местные анестетики, как ропивакаин и бупивакаин. К сожалению, у бупивакаина есть такие неприятные действия, как высокий риск выраженного моторного блока и вероятность кардиотоксических эффектов. Данные о сравнительной эффективности и безопасности применения ропивакаина и бупивакаина для обезболивания родов противоречивы (5-8). Некоторые авторы полагают, что ропивакаин вызывает меньший моторный блок, нежели бупивакаин (5,6), тогда как другие исследователи не выявили существенной разницы между этими двумя препаратами (7-9). Для того, чтобы избежать нежелательного моторного блока, можно использовать слабые растворы местных анестетиков в сочетании с наркотическими анальгетиками. Добавление фентанила к раствору местных анестетиков снижает дозу последних (и это зависит от дозы фентанила) (10).
Целью нашего исследования было изучение эффективности и побочных действий эпидуральной анестезии 0.0625% ропивакаина или бупивакаина с добавлением 2 мкг/мл фентанила для постоянной инфузии. Фентанил добавлялся к растворам местных анестетиков, поскольку он снижал потребность в них.
Методы
Данное проспективное, двойное слепое, рандомизированное исследование было одобрено местным этическим комитетом, от всех пациенток было получено письменное осознанное согласие. У пациенток, включенных в исследование, не было противопоказаний для регионарной анестезии, срок беременности у всех превышал 36 недель, масса тела была не более 100 кг, беременность была одноплодной, неосложненной, гипоксии плода зафиксировано не было. Пациентки с сахарным диабетом, неврологическими заболеваниями, кесаревым сечением в анамнезе, преэклампсией или аллергией исключались из исследования. Анестезиолог первых раз осматривал включенных в исследование женщин, когда они поступали в родильное отделение еще до того, как пациентки просили начать обезболивание. Затем пациентки случайным образом разделялись на две группы. После объяснения им сути исследования и получения согласия, проводилась оценка по шкале ASA , и в исследование включались только роженицы с оценкой I - II (всего 42 женщины). Все они находились в родах, раскрытие составляло 3-6 см, и у них были регулярные схватки по 1 минуте через 3-4 минуты. Ни одна пациентка не получала наркотических анальгетиков до проведения эпидуральной анестезии. Регистрировались следующие параметры: возраст, масса тела, рост, число родов, образование, срок беременности, раскрытие и применение окситоцина. Пациенты были случайным образом разделены на две группы: первая получала ропивакаин, вторая бупивакаин. Раствор препаратов приготавливал анестезиолог, который не имел непосредственного отношения к проведению регионарной анестезии, ведению пациенток или карт исследования, ни пациентки, ни врачи, выполняющие эпидуральную анестезию, не знали, какой именно раствор применяется.
До начала анестезии проводился мониторинг следующих параметров: систолическое и диастолическое артериальное давление, сатурация, и оценка по визуальной аналоговой шкале (0 = боли нет, 100 = боль нестерпимая). Мониторинг схваток и сердцебиения плода проводился с помощью внешнего монитора (Partoconter NST Nihon Kohden). До выполнения эпидуральной анестезии проводилась инфузия 500 мл раствора рингер-лактат. Эпидуральная анестезия выполнялась в положении сидя. В асептических условиях проводилась инфильтрационная анестезия кожи 2% раствором прокаина 2 мл, и в промежутке L2/3 или L3/4 выполнялась пункция эпидурального пространства по средней линии. Для идентификации положения кончика иглы (игла Туохи 18 G) использовался тест потери сопротивления с физраствором. Затем в эпидуральное пространство на 2-3 см в краниальном направлении проводился катетер (Perifix Soft Tip , B Braun ). После выполнения аспирационного теста вводилась тест-доза – 3 мл 2% лидокаина с добавлением адреналина 1:200 000. Если в течение 5 минут после этого не было признаков внутрисосудистого или интратекального введения препарата, начинали вводить первую болюсную дозу исследуемого препарата, она составляла 8 мл в концентрации 0.125% с добавлением 50 мкг фентанила (общий объем – 9 мл). Через 5 минут начинали постоянную инфузию 0.0625% раствора местного анестетика с добавлением фентанила 2 мкг/мл со скоростью 10 мл/час с помощью инфузомата (Flo - Gard 6301 dual channel volumetric infusion pump , Baxter). Уровень сенсорного блока оценивался с помощью исследования температурной чувствительности льдом до начала эпидуральной анестезии, а затем – через 5,10,20, 30, 45 и 60 минут после введения первой дозы местных анестетиков, а затем – каждые полчаса до рождения ребенка. Когда сенсорный блок был выше уровня Т10, скорость инфузии в эпидуральное пространство снижали до 8 мл/час, если уровень был ниже Т10, то дополнительно вводилась болюсная доза в 5 мл исследуемого препарата (0.0625% с добавлением фентанила 2 мкг/ мл) в эпидуральное пространство.
Степень моторного блока оценивалась по модифицированной шкале Bromage до выполнения эпидуральной анестезии и через 5,10,20, 30, 45 и 60 минут после введения первой дозы местных анестетиков, а затем – каждые полчаса до рождения ребенка (0 = нет моторного блока, 1 = невозможно согнуть бедро, 2 = невозможно согнуть ногу в коленном суставе, 3 = невозможность двигать ступней). Возможность ходить без посторонней помощи оценивалась по системе «да» - «нет». Если оценка по визуальной аналоговой шкале боли была более 40, то дополнительно вводились до двух блюсных доз в 5 мл исследуемого препарата (0.0625% с добавлением фентанила 2 мкг/ мл) в эпидуральное пространство. Пациенток исключали из исследования, если тест-доза выявляла введение препарата в просвет сосуда или в субарахноидальное пространство, аналгезия была неадекватной (было необходимо ввести более двух дополнительных доз местного анестетика), или если рождение ребенка происходило в первые 2 часа от начала анестезии.
В течение всего времени проведения исследования регистрировались следующие параметры: артериальное давление у матери, частота сердечных сокращений, сатурация, и сердцебиение плода – до выполнения анестезии, и 5,10,20, 30, 45 и 60 минут после введения первой дозы местных анестетиков, а затем – каждые полчаса до рождения ребенка. Гипотония – это снижение систолического артериального давления ниже 80% от исходного или менее 90 мм рт.ст., при регистрации гипотонии обязательно смещали матку влево от средней лини, увеличивали скорость внутривенного введения растворов, или внутривенно вводили эфедрин в дозе 3-5 мг. При брадикардии у плода (менее 120 уд/мин) также смещали матку влево от средней линии, давали матери кислород (10 л/мин через маску), вводили внутривенно растворы или эфедрин.
В карту исследования обязательно вносили такие данные, как продолжительность каждого периода родов, способ родоразрешения (самопроизвольные роды через естественные родовые пути, инструментальное родоразрешение через естественные родовые пути, кесарево сечение), общая доза использованного местного анестетика, оценка новорожденного по шкале Апгар на 1 и 5 минуте, оценка новорожденного по неврологическим и адаптивным шкалам ( NACS ) на втором и 24-ом часу жизни и данные исследования газов крови из пуповины (измерение проводилось с помощью анализатора U 0290008 P фирмы Nova biomedical ). В конце каждого периода родов обязательно оценивалось качество эпидуральной анестезии по мнению самой пациентки – очень хорошее (4), хорошее (3), удовлетворительное (2) или плохое (1). Анестезиологом фиксировались побочные эффекты и осложнения эпидуральной анестезии.
Статистический анализ выполнялся с помощью пакета SPSS для Windows 10.0, включающий тест Стьюдента, t -критерий, тест ? 2 и Wilcoxon . Также применялся тест Mann - Witney U для анализа непараметрических данных, например, оценки качества эпидуральной анестезии пациенткой и оценка по шкале Апгар. Результаты были представлены в виде средней и стандартной ошибки. Величина p < 0.05 считалась статистически достоверной.
Результаты
Первоначально в исследование были включены 42 пациентки (21 получала бупивакаина, и 21 – ропивакаин). Позднее две пациентки (по одной из каждой группы) были исключены из исследования, поэтому в окончательные данные вошли данные о 40 роженицах. Существенных различий по демографическими показателям и характеристикам течения родов в группах отмечено не было (Таблица 1).
Таблица 1. Демографические данные и характеристики родов.
| Группа, получавшая бупивакаин (20 женщин) |
Группа, получавшая ропивакаин (20 женщин) |
|
| Возраст (лет) | 25.05±0.64 | 25.35±0.96 |
| Рост (см) | 163.6±1.16 | 161.95±1.04 |
| Масса тела (кг) | 77.35±1.65 | 76.95±1.75 |
| Срок беременности (недель) | 38.55±0.28 | 38.95±0.31 |
| Раскрытие шейки матки (см) | 5.15±0.16 | 4.95±0.16 |
| Первородящие (%) | 65% | 60% |
| Повторнородящие (%) | 35% | |
| Применение окситоцина (%) | 45% | 40% |
| Образование | ||
| Начальная школа | 50% (10 женщин) | 55% (11 женщин) |
| Средняя школа | 40% (8 женщин) | 40% (8 женщин) |
| Высшее образование | 10% (2 женщины) | 5% (1 женщина) |
| Значения представлены в виде средних ± стандартное отклонение, статистически достоверных различий между группами не было. |
Разница как внутри групп, так и между группами по систолическому и диастолическому артериальному давлению, SpO2 , частоте сердечных сокращений у матери и частоте сердцебиения плода. Также была статистически незначительной.
Уровень сенсорного и моторного блока в обеих группах был одинаковым (Таблица 2). В обеих группах медиана потери чувствительности к уколам иглой по средне-ключичной линии была примерно одинаковой (Т8-10). У двух пациенток, получавших бупивакаин, развился односторонний моторный блок (2 степень по шкале 0-3). Ни у одной их рожениц не развился выраженный блок (степень 3). Все женщины могли ходить по родильной палате, если только к этому не было акушерских противопоказаний. Только у двух женщин (обе получали бупивакаин) ходить не получилось из-за резко выраженного моторного блока.
Таблица 2. Степень сенсорного и моторного блока
и число дополнительных доз местного анестетика
| Уровень блока | Группа, получавшая бупивакаин (20 женщин) |
Группа, получавшая ропивакаин (20 женщин) |
|
| Наивысший сенсорный блок (дерматом) | Т7 | 0 | 0 |
| Т8 | 2 | 2 | |
| Т9 | 16 | 14 | |
| Т10 | 2 | 4 | |
| Моторный блок (по шкале Bromage) | 0 | 18 | 20 |
| 1 | 0 | 0 | |
| 2 | 2 | 0 | |
| 3 | 0 | 0 | |
| Дополнительные болюсные дозы (число таких доз) | 2 | 14 | 13 |
| 1 | 5 | 5 | |
| 0 | 1 | 2 |
| Указаны числовые значения. Статистически достоверной разницы между группами не было. |
По общей дозе местного анестетика существенных различий между группами не было. Пациентки получили в среднем 30.17±1.48 мг бупивакаина и 31.20±1.96 мг ропивакаина до рождения ребенка (P >0.05). Средняя скорость введения препаратов составила 5.25 мл/час в группе, получавшей ропивакаин, и 5.125 мл/час в группе, получавшей бупивакаин ( P >0.05). Количество дополнительных болюсных введений местных анестетиков также не имело существенных отличий между группами (Таблица 2).
Оценки по визуальной аналоговой шкале боли были примерно одинаковыми. В обеих группах отмечено существенное снижение оценки по визуальной аналоговой шкале боли в течение первых пяти минут после введения первой дозы местного анестетика (P <0.05) (Рис. 1). Оценка по визуальной аналоговой шкале боли в момент рождения ребенка составила 51.5±2.3 в группе, где применялся бупивакаин, и 52.5±2.1 в группе, получавшей ропивакаин (P >0.05).
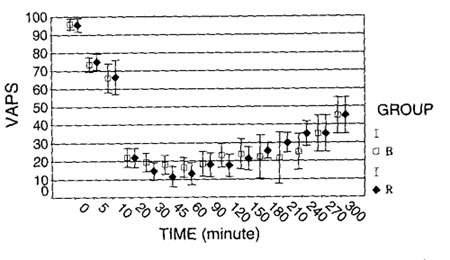 |
| Рисунок 1. Оценка по визуальной аналоговой шкале боли, значения представлены в виде средних ± стандартное отклонение, статистически достоверных различий между группами не было. По горизонтальной оси – время, по вертикальной оси – оценка по визуальной аналоговой шкале боли. Светлые квадраты – группа, получавшая бупивакаин, темные ромбы – группа, получавшая ропивакаин. |
Продолжительность первого периода родов фиксировалась с момента начала эпидуральной анестезии до полного раскрытия шейки матки. Продолжительность второго периода родов – это промежуток от полного раскрытия шейки матки до рождения ребенка. Существенной разницы по продолжительности первого и второго периода родов между группами отмечено не было (P >0.05) (Таблица 3). Также не отмечено существенных различий в способах родоразрешения, все пациентки родили самостоятельно. Никому не потребовалось выполнять кесарево сечение или инструментальное родоразрешение через естественные родовые пути (акушерские щипцы) (Таблица 3).
Таблица 3. Продолжительность родов и способ родоразрешения
| Группа, получавшая бупивакаин (20 женщин) |
Группа, получавшая ропивакаин (20 женщин) |
|
| Продолжительность I периода родов после начала эпидуральной анестезии (мин) | 124.75±11.06 | 140.00±11.36 |
| Продолжительность второго периода родов (мин) | 40.05±4.03 | 35.10±3.52 |
| Самостоятельное родоразрешение через естественные родовые пути (%) | 100% | 100% |
| Инструментальное родоразрешение (%) | 0 | 0 |
| Кесарево сечение (%) | 0 | 0 |
| Значения представлены в виде средних ± стандартное отклонение, статистически достоверных различий между группами не было. |
Существенной разницы в оценке качества обезболивания родов самими женщинами отмечено не было (P>0.05) (Рис. 2 и 3), однако все женщины отметили, что качество обезболивания было выше и им было комфортнее в первом периоде родов, а не во втором.
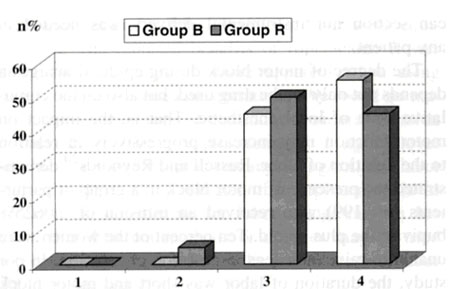 |
| Рисунок 2. Оценка качества обезболивания роженицами в течение первого периода родов. В общем, качество эпидуральной анестезии оценено женщинами, как очень хорошее (4 балла), хорошее (3 балла), удовлетворительное (2 балла) и плохое (1 балл). Данные представлены в виде относительных значений (%), статистически доствоерных различий между группами не получено. Светлые столбики – группа, получавшая бупивакаин, темные столбики – группа, получавшая ропивакаин. По горизонтали – оценка качества обезболивания, по вертикали - % женщин, давших такую оценку. |
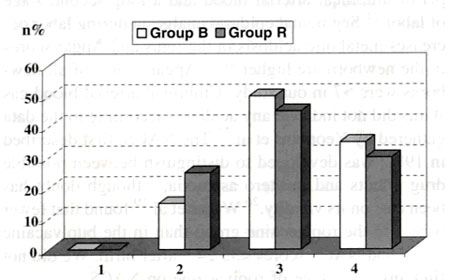 |
| Рисунок 3. Оценка качества обезболивания роженицами в течение второго периода родов. В общем, качество эпидуральной анестезии оценено женщинами, как очень хорошее (4 балла), хорошее (3 балла), удовлетворительное (2 балла) и плохое (1 балл). Данные представлены в виде относительных значений (%), статистически доствоерных различий между группами не получено. Светлые столбики – группа, получавшая бупивакаин, темные столбики – группа, получавшая ропивакаин. По горизонтали – оценка качества обезболивания, по вертикали - % женщин, давших такую оценку. |
Побочные эффекты и осложнения в обеих группах были одинаковы (P>0.05) (Таблица 4).
Таблица 4. Частота побочных эффектов и осложнений
| Группа, получавшая бупивакаин (20 женщин) |
Группа, получавшая ропивакаин (20 женщин) |
|
| Тяжелая гипотония | 0 | 0 |
| Тошнота и рвота | 0 | 1 |
| Кожный зуд | 3 | 4 |
| Боль в спине | 2 | 2 |
| Дрожь | 1 | 1 |
| Острая задержка мочи | 0 | 0 |
| Брадикардия у плода | 2 | 2 |
| Угнетение дыхания | 0 | 0 |
| Системное токсическое действие | 0 | 0 |
| Полный спинальный блок | 0 | 0 |
| Неврологический дефицит | 0 | 0 |
| Указаны числовые значения. Статистически достоверной разницы между группами не было. |
Ни у одной из пациенток не было зафиксировано падение артериального давления ниже 90 мм рт. ст. Самым частым побочным эффектом был легкий кожный зуд (у трех пациенток, получавших бупивакаин, и у 4 пациенток, получавших ропивакаин). Дрожь и кожный зуд не требовали никакого лечения и проходили самостоятельно. Брадикардия у плода (менее 120 уд/мин), продолжавшаяся более 40 секунд, отмечена у двух пациенток из каждой группы, и купировалась ингаляциями кислорода. Угнетение дыхания, системное токсическое действие и тотальный спинальный блок у женщин, включенных в исследование, не встречались.
Все новорожденные имели оценку по шкале Апгар 7 и более баллов, существенной разницы в состоянии новорожденных в двух группах отмечено не было (P >0.05) (Таблица 5). Анализ газов пуповинной крови также не имел существенных отличий (P >0.05). Оценка по шкале NACS на втором и 24 часу жизни у всех новорожденных была не менее 35, значительной разницы между группами также отмечено не было (P >0.05) (Таблица 5).
| Группа, получавшая бупивакаин (20 женщин) |
Группа, получавшая ропивакаин (20 женщин) |
|
| Оценка по шкале Апгар на 1 минуте | 9 (8-9) | 9 (8-10) |
| Оценка по шкале Апгар на 5 минуте | 10 (9-10) | 10 (10-10) |
| рН крови из артерии пуповины | 7.28±0.50 | 7.28 ±0.45 |
| РО2 (мм рт.ст) | 18.35±0.32 | 18.36±0.31 |
| РСО2 (мм рт.ст) | 49.59±0.39 | 49.92±0.29 |
| НСО3 (ммоль/л) | 21.75±0.20 | 22.06±0.20 |
| Оценка по шкале NACS через 2 часа | 37.15±0.16 | 37.00±0.20 |
| Оценка по шкале NACS через 24 часа | 39.25±0.16 | 39.05±0.18 |
| Указаны числовые значения. Статистически достоверной разницы между группами не было. |
Обсуждение
В последние годы наблюдается повсеместная тенденция к снижению применяемых концентраций растворов местных анестетиков для обезболивания родов. Некоторые исследователи сравнивали эффективность применения 0.25% растворов ропивакаина и бупивакаина, и не обнаружили никакой разницы в качестве обезболивания и характеристиках моторного и сенсорного блока (11,12). Owen с соавт. (7) сравнивали 0.125% раствор бупивакаина с добавлением 12 мкг/мл фентанила и такого же по концентрации раствора бупивакаина с фентанилом, которые применялись для эпидуральной анестезии, контролируемой пациенткой, никакой разницы между двумя препаратами выявлено не было. В другом исследовании изучалось применение болюсного введения 0.125% растворов бупивакаина и ропивакаина с добавлением суфентанила (9). Результаты этого исследования показали, что ропивакаин в сочетании с суфентанилом обеспечивал такое же по качеству обезболивание, что и бупивакаин с суфентанилом, однако моторный блок в этом случае был выражен меньше, и это не оказывало никакого влияния на течение родов и способ родоразрешения. Во всех этих публикациях авторы считают, что ропивакаин и бупивакаин одинаковы по мощности, однако в двух исследованиях было показано, что ропивакаин имеет мощность всего в 60% от мощности бупивакаина, когда его применяют для эпидуральной анестезии в родах (5,6). Polley с соавт. (5) и Capognia с соавт. (6) предположили, что минимальная концентрация раствора местного анестетика для ропивакаина и бупивакаина может быть показателем эффективности препарата. Минимальная концентрация раствора местного анестетика – это такая концентрация, при которой адекватная эпидуральная анестезия наступает у 50% пациентов. Также, Fernandez - Guiasola с соавт. (13) показали, что 0.0625% раствор бупивакаина с добавлением 2 мкг/мл фентанила и 0.1% раствор ропивакаина с добавлением 2 мкг/ мл фентанила оказывают клинически неразличимое действие, что позволяет предполагать, что ропивакаин действительно несколько слабее бупивакаина.
Перенос результатов трех вышеперечисленных исследований в клиническую практику должен осуществляться с осторожностью. Если ропивакаин слабее бупивакаина для обезболивания родов, то тогда необходимо применять его большие концентрации или объемы, чтобы обеспечить аналогичный уровень обезболивания родов, если считать, что кривые «доза-эффект» параллельны. Являются ли бупивакаин и ропивакаин на самом деле одинаковыми по мощности при использовании их в низких концентрациях? Именно для того, чтобы ответить на этот вопрос, мы и провели наше исследование. Мы использовали низкоконцентрированные (0.0625%) раствор ропивакаина и бупивакаина – эта концентрация примерно равна минимальной концентрации раствора местного анестетика (5,6). Минимальная концентрация раствора местного анестетика для бупивакаина с добавлением 2 мкг/мл фентанила составляет примерно 0.048% (10). Наши данные позволяют предполагать, что 0.0625% растворы бупивакаина и ропивакаина имеют одинаковую мощность. Возможно, разница между двумя местными анестетиками была несколько смазана, поскольку мы добавляли фентанил и тест-дозу лидокаина, что и могло повлиять на течение анестезии.
Связь между эпидуральной анестезией и оперативным родоразрешением часто является поводом для жарких споров. Моторный блок от эпидуральной анестезии может снижать возможность женщины передвигаться, уменьшать силу потуг и предрасполагать к неправильной ротации предлежащей части плода из-за расслабления мышц тазового дна (14, 15). Для эпидуральной анестезии в родах анестезиологи стараются использовать наименьшие возможные концентрации местных анестетиков, так, чтобы обеспечить адекватное обезболивание. Этого можно добиться либо понижением концентрации раствора местного анестетика, либо выбрав местный анестетик преимущественно с сенсорным, а не моторным блоком. Таким образом, можно будет снизить частоту инструментального родоразрешения или операций кесарева сечения (16-18). Некоторые исследователи обнаружили, что инструментальное родоразрешение реже встречается у рожениц, которые получали ропивакаин, чем у тех, кто получал бупивакаин (19). В нашем исследовании мы применяли наименьшие возможные концентрации местных анестетиков (0.625% с добавлением фентанила 2 мкг/мл) и не выявили никакой разницы в частоте инструментального родоразрешения между группами. Поскольку при таких низких концентрациях местного анестетика практически не развивается моторный блок, то и нарушений в течение второго периода родов не происходит.
Степень выраженности моторного блока во время эпидуральной анестезии зависит не только от используемого препарата, но и от общей его дозы. Поэтому моторный блок может постепенно нарастать с течением времени. Russelreynolds (20) показали, что при использовании 0.0625% бупивакаина в сочетании с наркотическим анальгетиком для инфузии в эпидуральное пространство в группе рожениц (199 женщин) мог развиваться моторный блок. Десять процентов пациенток не смогли поднимать ноги через 4-6 часов от начала инфузии. В нашем исследовании продолжительность родов была невелика, и моторный блок наблюдался только у 10% пациенток, получавших бупивакаин. Эта небольшая разница оказалась статистически недостоверной. Все это позволяет предположить, что при использовании низких концентраций растворов местных анестетиков разница в вероятности моторного блока между бупивакаином и ропивакаином невелика, поэтому более важным фактором вероятности возникновения моторного блока, по нашему мнению, может быть не сам препарат, а его концентрация или общая доза.
Потребность в обезболивании растет по мере хода родов. Мы выявили, что оценка по визуальной аналоговой шкале боли повышается к концу второго периода родов. Поскольку нами не отмечено никакой существенной разницы в оценке по шкале боли по данным нашего исследования, то мы сделали вывод, что клиническая эффективность малоконцентрированных растворов бупивакаина и ропивакаина одинакова. В этих дозах препараты давали одинаково хорошее обезболивание первого периода родов, но в конце второго периода и в момент рождения ребенка такой раствор не мог обеспечить полного обезболивания. Lyons с соавт. (10) показали, что в этом случае лучше применять фентанил в концентрации 3 мкг/мл, однако мы предпочли не увеличивать дозу фентанила олее, чем до 2 мкг/мл, поскольку это может вызывать нежелательный седативный эффект, тошноту и зуд.
Традиционно состояние новорожденного оценивается по шкале Апгар и результатам исследования кислотно-щелочного равновесия в пуповинной крови. Существует явная корреляция между рН крови из артерии пуповины и длительностью второго периода родов (21). Сегментарная эпидуральная анестезия в родах снижает степень метаболического ацидоза у плода, и повышает оценку по шкале Апгар у новорожденных (22,23). В нашем исследовании оценка всех новорожденных по шкале Апгар была выше 7 баллов. Исследование газов артериальной крови из артерии пуповины не выявило ацидоза, что соответствует данным, представленным в публикации Yeomans с соавт. (24). Шкала оценки состояния новорожденного NACS , которая впервые была описана в 1982 году, была разработана для того, чтобы отличить действие лекарственных препаратов от внутриутробной гипоксии и асфиксии (25), хотя имеются сомнения в ее действительности (26). Writer с соавт. (19) обнаружил, что в группе, получавшей ропивакаин, меньше детей имели оценку по шкале NACS менее 35 на 24-ом часу жизни, чем в группе, получавшей бупивакаин. Мы такой разницы выявить не смогли.
Таким образом, не отмечено существенной разницы в оценках по визуальной аналоговой шкале боли, общей дозе местного анестетика, степени сенсорного или моторного блока, побочным действиям, оценке качества обезболивания пациенткой, и исходам у новорожденных между двумя группами женщин, получавших либо бупивакаин, либо ропивакаин. Преимущества ропивакаина, описанные ранее (менее вероятный моторный блок) могут проявляться в случаях, когда используются более высокие концентрации местных анестетиков. В нашем исследовании мы смогли выявить, что ропивакаин также эффективен для обезболивания родов, как и бупивакаин. Мы считаем, что для того, чтобы повысить качество обезболивания родов во втором периоде следует применять разные режимы и методы регионарной анестезии.
Список литературы
- Glosren B . Anesthesia fur Obstetrics . In: Miller R D, editor. Anesthesia, 5th ed. vol. 2. New York : Churchill Livingstone, 2 (100 ) ; 2024-2086.
- Zlatnik F i. Obstetric management of labor and vaginal delivery. In: Chestnut D H. ed. Obstetric Anesthesia. 2nd ed. Si Louis: Mosby, 1999: 303-359.
- Moir D D. Local anaesthetic techniques in obstetrics. Br J Anaeslh 1986; 58: 747-759.
- Bonica S J. McDonald S J. The pain of childbirth. In: Bonica J J, ed. The Management of Pain. 2nded, Lea, Febiger; Philadelphia , 1990: 1313-1343.
- Policy L S, Columb M O, Naughton N N, Wagner D S. van de Ven C J. Relative analgesic potencies of ropivacaine and bupivacaine for epidural analgesia in labor: implications for therapeutic indexes. Anesthesiology 1999; 90: 944-950.
- Capogna G, Celleno D, Fusco P, Lyons G, Columb M. Relative potencies of bupivacaine and ropivacaine for analgesia in labour. BrJ Anaesth 1999; 82: 371-373.
- Owen M D, D'Angelo R. Gerancher J C, el al. 0.125% ropivacaine is similar to 0.125% bupivacaine lor labor analgesia using patient-controlled epidural infusion. Anesth Analg 1998; 86: 527-531.
- Meister G C, D^Angelo R. Owen M, Nelson K E, Gaver R. A comparison of epidural analgesia with 0.125% ropivacaine with fentanyl versus 0.125% bupivacaine with fentanyl during labor. Anesth Analg 2000; 90: 632-637.
- Gamier P, De Kock M, Van Steenberge A, Miclot D, Fanard L, Hody J L. A double-blind comparison of 0.125% ropivacaine with sufenlanil and 0.125% bupivacaine with sufenlanil for epidural labor analgesia. Ancsthesiology 1999; 90: 772-778.
- 10. Lyons G, Columb M, Hawthorne L, Dresner M. Extradural pain Velief in labour: bupivacaine sparing by extradural fentanyl is dose dependent, Br J Anaesth 1997; 78: 493^197.
- Stienstra R. Jonker T A, Bourdrez P, Kuijpsrs J C, van Kleef J W, Lundberg U, Ropivacaine 0.25% versus bupivacaine 0,25% for continuous epidural analgesia in labor: a double-blind comparison. Anesth Analg 1995; 80: 285-289.
- Muir H A. Writer D. Douglas J, Weeks S. Gambling D, Macarthur A. Double-blind comparison of epidural ropivacaine 0.25% and bupivacaine 0,25%, for the relief of childbirth pain. Can J Anacslh 1997; 44: 599-604.
- Fernandez-Guisasola J, SerranoM L, Cobo B, et al. A comparison of 0,0625% bupivacaine with fentanyl and 0.1% ropivacaine with fenlanyl for continuous epidural labor analgesia. Ancslh Analg 2001; 92: 1261-1265.
- Stoddart A P, Nicholson K E, Popham P A. Low dose bupivacaine/ fentanyl epidural infusions in labour and mode of delivery. Anaesthesia 1994; 49; 1087-1090.
- Goodfellow C F, Hull M G, Swaab D F. Dogterom J, Buijs R M. Oxytocin deficiency at delivery with epidural analgesia. Br J Obstet Gynaecol 1983; 90; 214-219.
- Vertommen J D. Vandermeulen E. Van Aken H. et al. The effects of addition of sufentanil to 0.125% bupivacaine on the quality of analgesia during labor and on the incidence of instrumental deliveries, Anesthesiology 1941; 74: 809-814.
- Chestnut D H. Does epidural analgesia during labor affect the incidence of cesarean delivery? Reg Aneslh 1997; 22: 495-499.
- Comparative Obstetric Mobile Epidural Trial (COMET) Study Group UK . Effect of low-dose mobile versus traditional epidural techniques on mode of delivery: a randomized controlled trial. Lancet 200l;358:19-23.
- Writer W D, Slienstra R, Eddleston J M, et al. Neonatal outcome and mode of delivery after epidural analgesia for labour with ropivacaine anil riupivucaine: a prospective meta-analysis. Br J Anaesth !9yS. Nl: 713-717.
- Russell R, Reynolds F. Epidural infusion of low-dose bupivacaine and opioid in labour; does- reducing motor block increase the spiiinaiK.'ini'. delivery rate? Anaesthesia 1996; 51; 266-273.
- Mongelli M. Wane C C, Wang W. Pang C C, Rogers M S. Oxygen free radical activity in the second stage of labor, Acta Obsiet Gynecol Scand 1997; 76: 765-768.
- Shyken J M. Smeltzer J S, Baxi L V, Blakemore K J, Ambrose S E, Pelrie R H. A comparison of the effect of epidural, general and no anesthesia on funic acid-base values by stage of labor and type of delivery. Am J Obstet Gynecol 1990; 163: 802-807.
- Reynolds F. Sharma S K, Seed P T. Analgesia in tahmir and fetal acid-base balance; a meta-analysis comparing epidural with systemic opioid analgesia. BJOG 2002; 109: 1344-1353.
- Yeomans E R, Hauth J C. Gilstrap L C, Strickland D M. Umbilical cord pH, PCO;, and bicarbonate following uncomplicated term vaginal deliveries. Am J Obstet Gynecol 1985; 151: 798-800.
- Arniel-Tison C, Barrier G. Shnider S M, Levinson G, Hughes S C. Stefani S J. A new neurologic and adaptive capacity scoring system for evaluating obstetric medications in full-term newborns. Anesthesiology 1982; 56; 340-350,
- Camann W, Brazelton T B. Use and abuse of neonalalneurobehavioral testing [editorial]. Anesthesiology 2000; 92: 3-5.
International Journal of Obstetric Anesthesia, 2005; 14: 288-293